题目内容
114号元素的一种同位素是由俄罗斯科学家合成的,存在时间只有30s,其质量数为289,该原子的中子数与电子数之差为
| A.61 | B.114 | C.175 | D.289 |
A
解析试题分析:根据质量数=质子数+中子数,可得中子数为289-114=175,质子数=电子数=114,可得中子数与电子数只差为175-114=61,选A。
考点:质量数、质子数、中子数,电子数之间的数量关系。

练习册系列答案
相关题目
某短周期金属元素原子核外最外层电子数是最内层电子数的1.5倍,下列说法正确的是( )
| A.该元素的单质性质活泼,具有较强的还原性,可以用于某些金属冶炼 |
| B.该元素的单质常温下不与浓硫酸反应 |
| C.该元素的单质无需特别保存,因为其性质稳定,不易与空气中的成分反应 |
| D.该元素的最高价氧化物对应的水化物只能与酸反应 |
X、Y两种元素形成含氧酸A和B,能说明酸A比酸B强的是
| A.酸A中X的非金属性比酸B中Y的非金属性强 |
| B.酸A中X与酸B中Y在同一周期,且X在Y之后 |
| C.酸A与酸B的铵盐溶液反应生成酸B |
| D.酸A具有强氧化性,酸B没有强氧化性 |
短周期元素X、Y、Z、W 的原子序数依次增大,且原子最外层电子数之和为13。X 的原子半径比Y 的小,X 与W 同主族,Z 是地壳中含量最高的元素。下列判断合理的是
| A.元素W分别与X、Y、Z形成的化合物都是离子化合物 |
| B.四种元素简单离子的半径:X < Y < Z < W |
| C.Z与其他三种元素形成的常见化合物中有离子晶体、原子晶体和分子晶体 |
| D.只含X、Y、Z 三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
重水(D2O)是重要的核工业原料,下列说法错误的是
| A.1H与D互称同位素 | B.1H→D通过化学变化不能实现 |
| C.H2O与D2O互称同素异形体 | D.1H218O与D216O的物理性质不同 |
不同元素的原子间最本质的区别是
| A.中子数不同 | B.相对原子质量不同 |
| C.质子数不同 | D.最外层电子数不同 |
重水 是重要的核工业原料,下列关于D原子的说法错误的是
是重要的核工业原料,下列关于D原子的说法错误的是
A.氘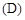 原子核外有1个电子 原子核外有1个电子 | B.是H的同位素 |
| C.自然界中没有D原子存在 | D.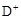 质量数为2 质量数为2 |
下列关于元素性质和结构的递变情况的说法错误的是( )
| A.Li、Be、B原子最外层电子数依次增多 |
| B.P、S、Cl元素最高正价依次升高 |
| C.N、O、F原子半径依次增大 |
| D.Na、K、Rb的电子层数逐渐增多 |