题目内容
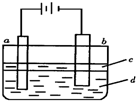
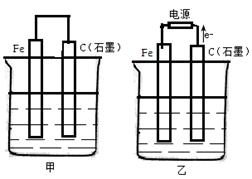
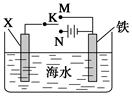
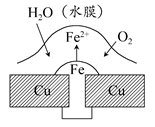
如下图各烧杯中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )
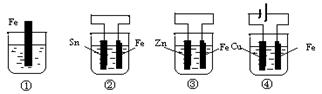

| A.④>②>①>③ | B.②>①>③>④ | C.④>②>③>① | D.③>②>④>① |
A
试题分析:以①作参照物,进行比较。在②中构成了原电池。由于活动性Fe>Sn,所以Fe作负极,加快了Fe的腐蚀,因此②>①,在③中构成了原电池。由于活动性Zn>Fe,所以Zn作负极,首先被腐蚀的的是Zn Fe得到了保护,腐蚀比原来慢。因此腐蚀速率①>③。④构成的是电解池,Fe是活性电极。由于Fe与电源的正极连接,作阳极,发生反应:Fe-2e-=Fe2+.腐蚀的速率比作原电池的负极还要快。因此腐蚀速率④>②。所以铁在其中被腐蚀时由快到慢的顺序是④>②>①>③ 。选项为A。

练习册系列答案
相关题目