题目内容
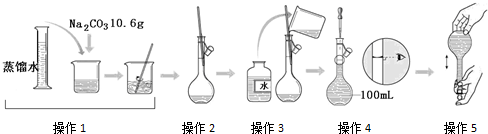
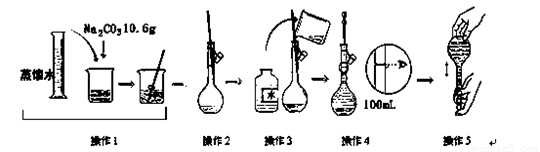
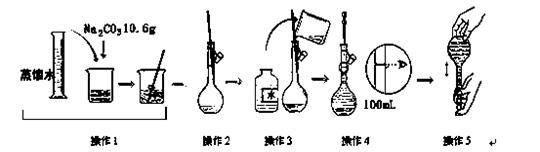
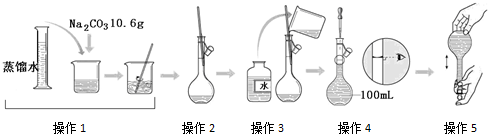
下图是配制一定物质的量浓度溶液的过程示意图.下列说法中错误的是( )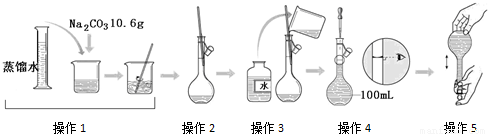
A.所配制的Na2CO3溶液的物质的量浓度为1.0 mol/L
B.操作2是将溶解的Na2CO3溶液转移到容量瓶中
C.操作4是滴加水至溶液凹液面的最低点与刻度线平齐
D.操作5定容摇匀后发现液面低于刻度线,要继续加水至液面与刻度线平齐
【答案】分析:A、由图可知,所配溶液的体积为100mL,根据n=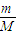 计算碳酸钠的物质的量,再根据c=
计算碳酸钠的物质的量,再根据c=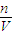 计算所配溶液的浓度;
计算所配溶液的浓度;
B、操作1是溶剂碳酸钠晶体,由图可知操作2是将溶解得到的碳酸钠溶液移入容量瓶;
C、操作4是定容,应滴加水至溶液凹液面的最低点与刻度线平齐;
D、定容摇匀后发现液面低于刻度线,少量溶液残留在瓶塞与瓶口之间,再加水至液面与刻度线平齐,导致所配溶液的体积偏大.
解答:解:A、由图可知,所配溶液的体积为100mL,10.6g碳酸钠的物质的量为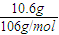 =0.1mol,所配碳酸钠溶液的浓度为
=0.1mol,所配碳酸钠溶液的浓度为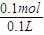 =1mol/L,故A正确;
=1mol/L,故A正确;
B、操作1是溶剂碳酸钠晶体,由图可知操作2是将溶解得到的碳酸钠溶液移入容量瓶,故B正确;
C、操作4是定容,应滴加水至溶液凹液面的最低点与刻度线平齐,故C正确;
D、定容摇匀后发现液面低于刻度线,少量溶液残留在瓶塞与瓶口之间,再加水至液面与刻度线平齐,导致所配溶液的体积偏大,所配溶液的浓度偏小,故D错误.
故选D.
点评:本题考查一定物质的量浓度溶液的配制,难度不大,注意根据c=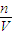 理解溶液的配制.
理解溶液的配制.
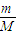 计算碳酸钠的物质的量,再根据c=
计算碳酸钠的物质的量,再根据c=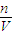 计算所配溶液的浓度;
计算所配溶液的浓度;B、操作1是溶剂碳酸钠晶体,由图可知操作2是将溶解得到的碳酸钠溶液移入容量瓶;
C、操作4是定容,应滴加水至溶液凹液面的最低点与刻度线平齐;
D、定容摇匀后发现液面低于刻度线,少量溶液残留在瓶塞与瓶口之间,再加水至液面与刻度线平齐,导致所配溶液的体积偏大.
解答:解:A、由图可知,所配溶液的体积为100mL,10.6g碳酸钠的物质的量为
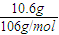 =0.1mol,所配碳酸钠溶液的浓度为
=0.1mol,所配碳酸钠溶液的浓度为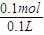 =1mol/L,故A正确;
=1mol/L,故A正确;B、操作1是溶剂碳酸钠晶体,由图可知操作2是将溶解得到的碳酸钠溶液移入容量瓶,故B正确;
C、操作4是定容,应滴加水至溶液凹液面的最低点与刻度线平齐,故C正确;
D、定容摇匀后发现液面低于刻度线,少量溶液残留在瓶塞与瓶口之间,再加水至液面与刻度线平齐,导致所配溶液的体积偏大,所配溶液的浓度偏小,故D错误.
故选D.
点评:本题考查一定物质的量浓度溶液的配制,难度不大,注意根据c=
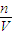 理解溶液的配制.
理解溶液的配制. 
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目