题目内容
已知:H2(g)+I2(g)  2HI(g);ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
2HI(g);ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
A.甲、乙提高相同温度
B.甲中加入0.1 mol He,乙不变
C.甲降低温度,乙不变
D.甲增加0.1 mol H2,乙增加0.1 mol I2
【答案】
C
【解析】
试题分析:恒温、恒压条件下,起始甲、乙投入量相当,是等效平衡,平衡状态相同。升高相同温度,平衡移动情况相同,仍然相等,A错。甲中加入0.1 mol He,平衡不移动,仍相等,B错。对甲降温,平衡正移,则甲中c(HI)增大,C对。甲、乙分别增加0.1 mol H2、0.1 mol I2,平衡同等程度地正移,二者仍相等,D错,所以答案选C。
考点:考查勒·夏特列原理的应用及“等效平衡”的判断
点评:该题是高考中的常见题型和考点,属于中等难度试题的考查。试题难易适中,综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确等效平衡的含义以及判断依据,然后结合题意灵活运用即可。

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
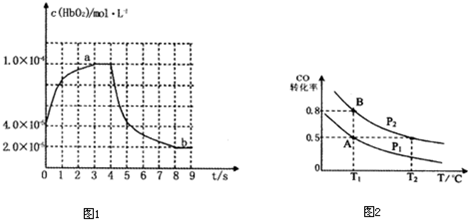
 (2010?山东)硫一碘循环分解水制氢主要涉及下列反应:
(2010?山东)硫一碘循环分解水制氢主要涉及下列反应: H2+I2
H2+I2 2HI(g)的平衡常数K=
2HI(g)的平衡常数K=