题目内容
质量分数为w1、物质的量浓度为c1的硫酸溶液与质量分数为w2、物质的量浓度为c2的硫酸溶液相比,如w1=2w2,则c1与c2的关系正确的是
- A.c1=2c2
- B.c1>2c2
- C.c1<2c2
- D.c2<c1<2c2
B
分析:浓硫酸的密度大于水,溶液的浓度越大,密度越大,利用c=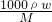 进行判断.
进行判断.
解答:设物质的量是浓度为c1 mol?L-1的密度为ρ1,物质的量是浓度为c2mol?L-1硫酸溶液的密度为ρ2,则
c1= ,c2=
,c2=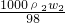 ,
,
 =
=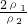
因浓硫酸的密度大于水,溶液的浓度越大,密度越大,则ρ1>ρ2,
则c1>2c2,
故选B.
点评:本题考查物质的量浓度与质量分数的计算与比较,题目难度中等,注意浓硫酸的密度大于水,溶液的浓度越大,密度越大.
分析:浓硫酸的密度大于水,溶液的浓度越大,密度越大,利用c=
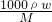 进行判断.
进行判断.解答:设物质的量是浓度为c1 mol?L-1的密度为ρ1,物质的量是浓度为c2mol?L-1硫酸溶液的密度为ρ2,则
c1=
 ,c2=
,c2=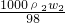 ,
, =
=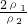
因浓硫酸的密度大于水,溶液的浓度越大,密度越大,则ρ1>ρ2,
则c1>2c2,
故选B.
点评:本题考查物质的量浓度与质量分数的计算与比较,题目难度中等,注意浓硫酸的密度大于水,溶液的浓度越大,密度越大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目