题目内容
下列有关物质结构的说法正确的是( )
| A、78g Na2O2晶体中所含阴、阳离子个数均为4NA |
| B、3.4g氨气中含有0.6NA个N-H键 |
C、HBr的电子式为H+ |
| D、PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 |
考点:离子晶体,电子式,物质结构中的化学键数目计算,原子核外电子排布
专题:原子组成与结构专题,化学键与晶体结构
分析:A、根据过氧化钠的物质的量以及1个过氧化钠中含有2个阳离子和1个阴离子;
B、根据氨气的物质的量以及1个氨气中含有3个N-H键;
C、根据溴化氢为共价化合物,氢原子与溴原子形成一对共用电子对,溴化氢中溴原子最外层达到8电子稳定结构,氢原子最外层为2个电子;
D、对于共价化合物元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构;
B、根据氨气的物质的量以及1个氨气中含有3个N-H键;
C、根据溴化氢为共价化合物,氢原子与溴原子形成一对共用电子对,溴化氢中溴原子最外层达到8电子稳定结构,氢原子最外层为2个电子;
D、对于共价化合物元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构;
解答:
解:A、78g Na2O2晶体的物质的量为
=1mol,1个过氧化钠中含有2个阳离子和1个阴离子,78g Na2O2晶体中所含阴、阳离子个数分别为2NA、NA,故A错误;
B、3.4g氨气的物质的量为
=0.2mol,1个氨气中含有3个N-H键,所以3.4g氨气中含有0.6NA个N-H键,故B正确;
C、溴化氢为共价化合物,氢原子与溴原子形成了一个共用电子对,溴化氢中氢原子最外层为2个电子,溴原子最外层达到8电子,用小黑点表示原子最外层电子,则溴化氢的电子式为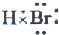 ,故C错误;
,故C错误;
D、PCl3中P元素化合价为+3价,P原子最外层电子数是5,3+5=8,则P原子满足8电子结构,Cl元素化合价绝对值为1,其最外层电子数是7,1+7=8,则Cl原子满足8电子结构;BF3中B元素化合价为+3,Be原子最外层电子数为3,所以3+3=6,分子中Be原子不满足8电子结构,故D错误;
故选B.
| 78g |
| 78g/mol |
B、3.4g氨气的物质的量为
| 3.4g |
| 17g/mol |
C、溴化氢为共价化合物,氢原子与溴原子形成了一个共用电子对,溴化氢中氢原子最外层为2个电子,溴原子最外层达到8电子,用小黑点表示原子最外层电子,则溴化氢的电子式为
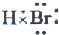 ,故C错误;
,故C错误;D、PCl3中P元素化合价为+3价,P原子最外层电子数是5,3+5=8,则P原子满足8电子结构,Cl元素化合价绝对值为1,其最外层电子数是7,1+7=8,则Cl原子满足8电子结构;BF3中B元素化合价为+3,Be原子最外层电子数为3,所以3+3=6,分子中Be原子不满足8电子结构,故D错误;
故选B.
点评:本题主要考查物质的构成、电子式的书写、8电子结构的判断等,难度不大,注意物质的结构.

练习册系列答案
相关题目
微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极总反应为:Zn+Ag2O+H2O═Zn(OH)2+2Ag;根据上述反应式,判断下列叙述中正确的是( )
| A、在使用过程中,电池负极区溶液的pH增大 |
| B、电子由Ag20极经外电路流向Zn极 |
| C、负极失去1mol电子时,正极生成108g银 |
| D、Zn电极发生还原反应,Ag2O电极发生氧化反应 |
下列各组物质间的反应与反应类型不相符的是( )
| A、乙烯与溴水(加成反应) |
| B、苯与浓硝酸(硝化反应) |
| C、氯乙烷与氢氧化钠醇溶液 (取代反应) |
| D、乙稀与高锰酸钾(氧化反应) |
下列物质属于电解质的是( )
| A、蔗糖 |
| B、盐酸 |
| C、SO2 |
| D、硫酸钡 |
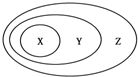 用如图表示的一些物质或概念之间的从属或包含关系中不正确的是( )
用如图表示的一些物质或概念之间的从属或包含关系中不正确的是( )| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 含氧酸 | 酸 | 化合物 |
| B | 溶液 | 分散系 | 混合物 |
| C | 强电解质 | 电解质 | 化合物 |
| D | 单质 | 化合物 | 纯净物 |
| A、A | B、B | C、C | D、D |
下列说法中肯定错误的是( )
| A、某原子K层上只有一个电子 |
| B、某原子M层上电子数为L层电子数的4倍 |
| C、某离子M层上和L层上的电子数均为K层的4倍 |
| D、阳离子的最外层电子数可能为2,也可能为8 |
对符号
Cl的理解正确的是( )
35 17 |
| A、氯元素的一种原子的相对原子质量是35 |
| B、氯元素的一种原子的质子数是35 |
| C、氯元素的一种原子的质量数是17 |
| D、氯元素的一种原子的原子核内中子数是18 |
海洋中有丰富的食品、矿产、能源、药物和水产资源,对今后世界经济发展有着决定性作用.下列有关说法正确的是( )


| A、整个过程可在实验室中模拟进行 |
| B、工段②是风化过程 |
| C、在工段③④⑤中溴元素均被氧化 |
| D、工段①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |