��Ŀ����
��ѧ̽��С����H2C2O4�����ᣩ��Һ�ⶨKMnO4��Һ��Ũ�ȣ���ش��������⣺
I��ȡ20.00mL0.250mol/L H2C2O4����Һ������ƿ�У���������ϡ�����ữ����KMnO4��Һ���еζ����ζ���Ӧ����ʽΪ��δ��ƽ����
KMnO4+H2C2O4+H2SO4��K2SO4+MnSO4+CO2��+H2O
��¼�������£�
��1���ζ�ʱ��KMnO4��ҺӦװ��______�ζ����У�ѡ���ʽ����ʽ����
��2���ζ��յ���жϷ����ǣ�______��
��3�������������ݼ��㣬��KMnO4��Һ��Ũ��Ϊ______mol/L��
��4�����в�����ʹ��KMnO4��ҺŨ��ƫ�͵���______��
A���ζ�����ˮϴ����ֱ��ע��KMnO4��Һ
B���ζ�ǰʢ�ű�H2C2O4��Һ����ƿ������ˮϴ����û�и���
C���ζ������ڵζ�ǰ�����ݣ��ζ���������ʧ
D����ȡKMnO4��Һ���ʱ���ζ�ǰƽ�ӣ��ζ��������Ӷ���
II���ζ��з��֣�KMnO4�Ϻ�ɫ��ȥ���ٶȿ�ʼʱ������������졢����ֱ�����Ϊ�о����������ԭ��ͬѧ��������������ʵ�飬ʵ���������±���
��5�������������ݣ���ȷ�������з�Ӧ������������ĺ���������______��
I��ȡ20.00mL0.250mol/L H2C2O4����Һ������ƿ�У���������ϡ�����ữ����KMnO4��Һ���еζ����ζ���Ӧ����ʽΪ��δ��ƽ����
KMnO4+H2C2O4+H2SO4��K2SO4+MnSO4+CO2��+H2O
��¼�������£�
| �ζ����� | ����Һ���/mL | ������Һ���/mL | |
| �ζ�ǰ�̶� | �ζ���̶� | ||
| 1 | 20.00 | 1.50 | 23.70 |
| 2 | 20.00 | 1.02 | 21.03 |
| 3 | 20.00 | 2.00 | 21.99 |
��2���ζ��յ���жϷ����ǣ�______��
��3�������������ݼ��㣬��KMnO4��Һ��Ũ��Ϊ______mol/L��
��4�����в�����ʹ��KMnO4��ҺŨ��ƫ�͵���______��
A���ζ�����ˮϴ����ֱ��ע��KMnO4��Һ
B���ζ�ǰʢ�ű�H2C2O4��Һ����ƿ������ˮϴ����û�и���
C���ζ������ڵζ�ǰ�����ݣ��ζ���������ʧ
D����ȡKMnO4��Һ���ʱ���ζ�ǰƽ�ӣ��ζ��������Ӷ���
II���ζ��з��֣�KMnO4�Ϻ�ɫ��ȥ���ٶȿ�ʼʱ������������졢����ֱ�����Ϊ�о����������ԭ��ͬѧ��������������ʵ�飬ʵ���������±���
| ��� | �¶�/�� | �ữ��H2C2O4��Һ/mL | KMnO4��Һ/mL | ��Һ��ɫʱ��/s |
| 1 | 25 | 5.0 | 2.0 | 40 |
| 2 | 25 | 5.0�����������MnSO4��ĩ�� | 2.0 | 4 |
| 3 | 60 | 5.0 | 2.0 | 25 |
I����1��KMnO4��Һ����ǿ�����ԣ����Ը�ʴ��Ƥ�ܣ�Ӧװ����ʽ�ζ����У�
�ʴ�Ϊ����ʽ��
��2�����ᷴӦ��ϣ��������һ��KMnO4��Һ����Һ��Ϊ��ɫ����ɫ30s�ڲ���ȥ��˵���ζ����յ㣻
�ʴ�Ϊ���������һ��KMnO4��Һ����Һ��Ϊ��ɫ����30s�ں�ɫ����ȥ��
��3����1��KMnO4��Һ��������2��3�����Ƚϴ�Ӧ�����Ӧ����2��3���������KMnO4��Һ�������������KMnO4��Һ�����Ϊ
=20mL����KMnO4��Һ��Ũ��Ϊcmol/L����2KMnO4��5H2C2O4��֪��20mL��cmol/L=
��20mL��0.250mol/L�����c=0.100��
�ʴ�Ϊ��0.100��
��4���ɹ�ϵʽ2KMnO4��5H2C2O4��֪V��KMnO4��?c��KMnO4��=
V��H2C2O4��?c��H2C2O4������c��KMnO4��=
A���ζ�����ˮϴ����ֱ��ע��KMnO4��Һ�����������Һ��ϡ�ͣ�ʹ�õĸ��������Һ�����ƫ�ⶨ�ĸ�����ص�Ũ��ƫ�ͣ���A���ϣ�
B����ƿ������ˮϴ����û�и���Բ�������ʵ���û��Ӱ�죬�ʶԲⶨ�ĸ�����ص�Ũ����Ӱ�죬��B�����ϣ�
C���ζ������ڵζ�ǰ�����ݣ��ζ���������ʧ���������Ը��������Һ���������ƫ�ⶨ�ĸ�����ص�Ũ��ƫ�ͣ���C���ϣ�
D����ȡKMnO4��Һ���ʱ���ζ�ǰƽ�ӣ��ζ��������Ӷ������������Ը��������Һ���������ƫС���ⶨ�ĸ�����ص�Ũ��ƫ�ߣ���D�����ϣ�
��ѡAC��
��5���Աȵ�1��2��ʵ�飬��2��ʵ�����MnSO4����ɫʱ��̣���Ӧ���ʿ죬˵��Mn2+�Է�Ӧ���д����ã��Աȵ�1��3��ʵ�飬��3��ʵ���¶����ߣ���ɫʱ��̣���Ӧ���ʿ죬˵���¶����ߣ���Ӧ���ʼӿ죬�ɴ˿�֪���������ԭ���ǣ���Ӧ���ɵ�Mn2+�Է�Ӧ��������ã���Ӧ����ʹ�¶����ߣ��ӿ췴Ӧ���ʿ죻
�ʴ�Ϊ����Ӧ���ɵ�Mn2+�Է�Ӧ��������ã���Ӧ����ʹ�¶����ߣ��ӿ췴Ӧ���ʿ죻
�ʴ�Ϊ����ʽ��
��2�����ᷴӦ��ϣ��������һ��KMnO4��Һ����Һ��Ϊ��ɫ����ɫ30s�ڲ���ȥ��˵���ζ����յ㣻
�ʴ�Ϊ���������һ��KMnO4��Һ����Һ��Ϊ��ɫ����30s�ں�ɫ����ȥ��
��3����1��KMnO4��Һ��������2��3�����Ƚϴ�Ӧ�����Ӧ����2��3���������KMnO4��Һ�������������KMnO4��Һ�����Ϊ
| (21.03-1.02)mL+(21.99-2.00)mL |
| 2 |
| 2 |
| 5 |
�ʴ�Ϊ��0.100��
��4���ɹ�ϵʽ2KMnO4��5H2C2O4��֪V��KMnO4��?c��KMnO4��=
| 2 |
| 5 |
| ||
| V(KMnO4) |
A���ζ�����ˮϴ����ֱ��ע��KMnO4��Һ�����������Һ��ϡ�ͣ�ʹ�õĸ��������Һ�����ƫ�ⶨ�ĸ�����ص�Ũ��ƫ�ͣ���A���ϣ�
B����ƿ������ˮϴ����û�и���Բ�������ʵ���û��Ӱ�죬�ʶԲⶨ�ĸ�����ص�Ũ����Ӱ�죬��B�����ϣ�
C���ζ������ڵζ�ǰ�����ݣ��ζ���������ʧ���������Ը��������Һ���������ƫ�ⶨ�ĸ�����ص�Ũ��ƫ�ͣ���C���ϣ�
D����ȡKMnO4��Һ���ʱ���ζ�ǰƽ�ӣ��ζ��������Ӷ������������Ը��������Һ���������ƫС���ⶨ�ĸ�����ص�Ũ��ƫ�ߣ���D�����ϣ�
��ѡAC��
��5���Աȵ�1��2��ʵ�飬��2��ʵ�����MnSO4����ɫʱ��̣���Ӧ���ʿ죬˵��Mn2+�Է�Ӧ���д����ã��Աȵ�1��3��ʵ�飬��3��ʵ���¶����ߣ���ɫʱ��̣���Ӧ���ʿ죬˵���¶����ߣ���Ӧ���ʼӿ죬�ɴ˿�֪���������ԭ���ǣ���Ӧ���ɵ�Mn2+�Է�Ӧ��������ã���Ӧ����ʹ�¶����ߣ��ӿ췴Ӧ���ʿ죻
�ʴ�Ϊ����Ӧ���ɵ�Mn2+�Է�Ӧ��������ã���Ӧ����ʹ�¶����ߣ��ӿ췴Ӧ���ʿ죻

��ϰ��ϵ�д�
 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
�����Ŀ
 Fe2++Ag+����ش��������⣺
Fe2++Ag+����ش��������⣺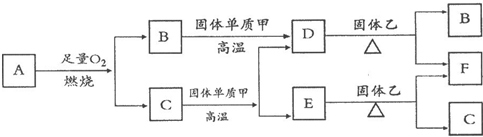
 ��ˮ��Ӧ������Ȳ��
��ˮ��Ӧ������Ȳ�� ��
��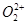 ��Ϊ�ȵ����壬
��Ϊ�ȵ����壬 ����ĿΪ_ ��
����ĿΪ_ �� ��Ԫ�س����������ۣ�����������������������������������������������������ͬѧͬʱ���ʵ�鷽������֤���Ʋ��Ƿ���ȷ�������ʵ�鷽���������������������� ��
��Ԫ�س����������ۣ�����������������������������������������������������ͬѧͬʱ���ʵ�鷽������֤���Ʋ��Ƿ���ȷ�������ʵ�鷽���������������������� �� ���л��ϳɹ�ҵ��һ��ԭ�ϡ���ҵ������
���л��ϳɹ�ҵ��һ��ԭ�ϡ���ҵ������ ��ˮ��Ӧ������Ȳ��
��ˮ��Ӧ������Ȳ�� ��
�� ��Ϊ�ȵ����壬
��Ϊ�ȵ����壬 ��ʾΪ ��1mol
��ʾΪ ��1mol  ����ĿΪ_ ��
����ĿΪ_ ��