题目内容
【题目】下列各图与表述一致的是( )
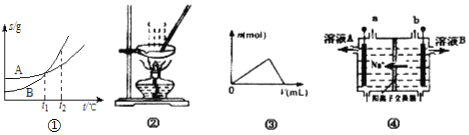
A. 图①表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B饱和溶液分别升温至t2℃时,溶质的质量分数B>A
B. 用图②所示装置蒸发FeCl3溶液制备无水FeCl3
C. 图③可以表示向一定量的明矾溶液中逐滴摘加一定浓度氢氧化钡溶液时产生Al(OH)3沉淀的物质的量变化
D. 图④电解饱和食盐水的装置中,溶液A、B中由水电离出的c(H+):A>B
【答案】C
【解析】A. 图①表示A、B两物质的溶解度随温度变化情况,将t1℃时,A和B的溶解度相同,A、B饱和溶液分别升温至t2℃时,两溶液变为不饱和溶液,所以溶质的质量分数B=A,A不正确;B. 蒸发FeCl3溶液制备无水FeCl3必须在氯化氢的气流中才能完成,直接蒸发因促进氯化铁水解,B不正确;C. 铝离子与氢氧根反应,物质的量之比为1:3时氢氧化铝沉淀达到最大量,物质的量之比为1:4时氢氧化铝沉淀完全溶解,图③可以表示向一定量的明矾溶液中逐滴摘加一定浓度氢氧化钡溶液时产生Al(OH)3沉淀的物质的量变化,C正确;D. 由图④中钠离子的运动方向可知,左边为阴极室,右边为阳极室,电解饱和食盐水的装置中,溶液A为浓氢氧化钠溶液、B为食盐水,所以由水电离出的c(H+):A<B,D不正确。本题选C。

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目