题目内容
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约为 mol·L-1。
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)= mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是 (填序号)。
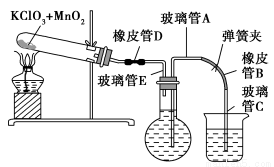
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0 g

(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2 000 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为 mol·L-1。
②需用浓硫酸的体积为 mL。
(1)4.0 (2)0.04 (3)C (4)①4.6 ②250
【解析】(1)由c=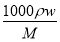 得,c(NaClO)=
得,c(NaClO)=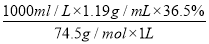 ≈4.0(mol·L-1)。
≈4.0(mol·L-1)。
(2)稀释前后溶液中NaClO的物质的量不变,则有:100 mL×10-3 L·mL-1×4.0 mol·L-1=100 mL×100×10-3 L·mL-1×c(NaClO),解得稀释后c(NaClO)=0.04 mol·L-1,c(Na+)=c(NaClO)=0.04 mol·L-1。(3)选项A,需用托盘天平称量NaClO固体,需用烧杯来溶解NaClO,需用玻璃棒进行搅拌和引流,需用容量瓶和胶头滴管来定容,图示的A、B不需要,但还需玻璃棒和胶头滴管。选项B,配制过程中需要加入水,所以经洗涤干净的容量瓶不必烘干后再使用。选项C,未洗涤烧杯和玻璃棒将导致配制的溶液中溶质的物质的量减小,结果偏低。选项D,应选取500 mL的容量瓶进行配制,然后取出480 mL即可,所以需要NaClO的质量:0.5 L×4.0 mol·L-1×74.5 g·mol-1=149.0 g。(4)①根据H2SO4的组成可知,溶液中c(H+)=2c(H2SO4)=4.6 mol·L-1。②2 000 mL 2.3 mol·L-1的稀硫酸中溶质的物质的量为2 L×2.3 mol·L-1=4.6 mol,设需要98%(密度为1.84 g·cm-3)的浓硫酸的体积为V mL,则有: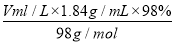 =4.6 mol,解得V=250。
=4.6 mol,解得V=250。