题目内容
已知反应KClO3+6HCl=KCl+3C12↑+3H2O,若用K35ClO3和H37C1作用,则下列说法正确的是( )A.生成的氯气式量约为73.3
B.KCl中只含有35C1
C.KCl中既有35Cl,又含37C1
D.该反应中转移电子数为6
【答案】分析:A、根据氯气的组成核素计算其式量.
B、根据氯化氢和氯化钾中氯元素的化合价判断氯化钾中氯元素的来源,从而判断选项的正误.
C、根据氯化氢和氯化钾中氯元素的化合价判断氯化钾中氯元素的来源,从而判断选项的正误.
D、根据化合价的变化判断转移电子.
解答:解:A、根据KClO3+6HCl=KCl+3C12↑+3H2O知,3个氯气分子含有的6个氯原子有1个35Cl原子和5个37C1原子,所以氯气式量约=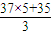 =73.3,故A正确.
=73.3,故A正确.
B、氯化氢中的氯元素和氯化钾中的氯元素化合价相同,所以氯化钾中的氯元素来源于氯化氢,氯化钾中只含有
37C1,故B错误.
C、氯化氢中的氯元素和氯化钾中的氯元素化合价相同,所以氯化钾中的氯元素来源于氯化氢,氯化钾中只含有
37C1,故C错误.
D、该反应中电子数转移为5,故D错误.
故选A.
点评:本题以氧化还原反应为载体考查了同位素,难度不大,会根据化合价的变化判断元素的来源是解本题的关键.
B、根据氯化氢和氯化钾中氯元素的化合价判断氯化钾中氯元素的来源,从而判断选项的正误.
C、根据氯化氢和氯化钾中氯元素的化合价判断氯化钾中氯元素的来源,从而判断选项的正误.
D、根据化合价的变化判断转移电子.
解答:解:A、根据KClO3+6HCl=KCl+3C12↑+3H2O知,3个氯气分子含有的6个氯原子有1个35Cl原子和5个37C1原子,所以氯气式量约=
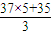 =73.3,故A正确.
=73.3,故A正确.B、氯化氢中的氯元素和氯化钾中的氯元素化合价相同,所以氯化钾中的氯元素来源于氯化氢,氯化钾中只含有
37C1,故B错误.
C、氯化氢中的氯元素和氯化钾中的氯元素化合价相同,所以氯化钾中的氯元素来源于氯化氢,氯化钾中只含有
37C1,故C错误.
D、该反应中电子数转移为5,故D错误.
故选A.
点评:本题以氧化还原反应为载体考查了同位素,难度不大,会根据化合价的变化判断元素的来源是解本题的关键.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目