题目内容
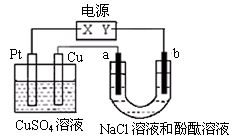
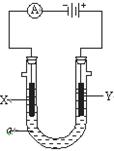
在100 mLCuSO4的溶液中,用石墨作电极电解一段时间,两极均收到2.24L气体(标准状况),则原溶液中,Cu2+的物质的量浓度为 ( )
| A.1mol?L―1 | B.2mol?L―1 | C.3 mol?L―1 | D.4 mol?L―1 |
A
考查电解池的有关计算和电极产物的判断。惰性电极电解硫酸铜溶液,阳极失去电子,OH-放电,发生氧化反应生成氧气,电极反应式为4OH--4e-=2H2O+O2↑。阴极铜离子放电,发生还原反应析出单质铜,电极反应式为2Cu2++4e-=2Cu。应用两极均收集到气体,说明铜离子不足,当铜离子放电完毕之和,溶液中的氢离子开始在阴极放电,电极反应式为4H++4e-=2H2↑。氧气和氢气的物质的量都是0.1mol,所以根据电子得失是知铜离子的物质的量应是0.1mol,所以浓度是1.0mol/L。答案是A。

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目