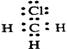题目内容
下列电子式中错误的是( )
分析:分析所给微粒类型,根据化学键类型及原子间形成共用电子对数目解答.
解答:解:A、碳原子最外层有4个电子,要达到稳定结构要形成四对共用电子对,电子式为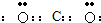 而,题中给出的电子式中碳原子只有两对共用电子对,故A错误;
而,题中给出的电子式中碳原子只有两对共用电子对,故A错误;
B、氢氧根是原子团阴离子,要用中括号括起来,并在右上角表明电荷数,因氧原子最外层6个电子,氢原子最外层1个电子,则OH-的电子式为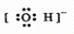 ,故B正确;
,故B正确;
C、因Na+是简单阳离子,它的电子式就是它的离子符号,故C正确;
D、氮原子最外层有5个电子,要达到稳定结构得形成三对共用电子对,电子式为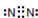 ,故D正确.
,故D正确.
故选:A.
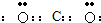 而,题中给出的电子式中碳原子只有两对共用电子对,故A错误;
而,题中给出的电子式中碳原子只有两对共用电子对,故A错误;B、氢氧根是原子团阴离子,要用中括号括起来,并在右上角表明电荷数,因氧原子最外层6个电子,氢原子最外层1个电子,则OH-的电子式为
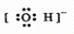 ,故B正确;
,故B正确;C、因Na+是简单阳离子,它的电子式就是它的离子符号,故C正确;
D、氮原子最外层有5个电子,要达到稳定结构得形成三对共用电子对,电子式为
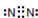 ,故D正确.
,故D正确.故选:A.
点评:本题考查化学用语的使用,学生明确原子的最外层电子数及物质的类别、电子式的书写方法是解答本题的关键.

练习册系列答案
相关题目
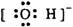 C.
C.
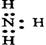 D.
D.