题目内容
已知分子E和分子G反应,生成两种分子L和M(组成E、G、L、M分子的元素原子序数小于10 “○”代表原子“—”表示化学键),如下图,则下列判断错误的是(未配平)


| A.G是最活泼的非金属单质 | B.L中的化学键是极性键 |
| C.E能使紫色的石蕊试液变蓝 | D.M的化学性质活泼 |
D
由图,得:E为三角锥结构,故为氨分子;G、L均为双原子分子;M中两原子间形成三键,故M为氮分子;说明是氨气被氧化成氮气,所以反应为:NH3+F2→HF+N2(未配平);
F原子得电子能力最强,则元素的非金属性最强,A正确;
HF中不同原子间形成极性共价键,故B正确;
氨气溶于水生成一水合氨,能电离出OH-,显碱性,则能使紫色的石蕊试液变蓝,C正确;
氮分子中存在氮、氮三键,作用力较大,故氮分子的化学性质应比较稳定,故D错误;
F原子得电子能力最强,则元素的非金属性最强,A正确;
HF中不同原子间形成极性共价键,故B正确;
氨气溶于水生成一水合氨,能电离出OH-,显碱性,则能使紫色的石蕊试液变蓝,C正确;
氮分子中存在氮、氮三键,作用力较大,故氮分子的化学性质应比较稳定,故D错误;

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
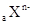 和
和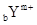 两种离子,其电子层结构相同。下列关系式或化学式正确的是
两种离子,其电子层结构相同。下列关系式或化学式正确的是