题目内容
【题目】某强酸性溶液X中可能含有Fe2+、A13+、NH4+、CO32-、SO32-、SO42-、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如下,下列说法不正确的是
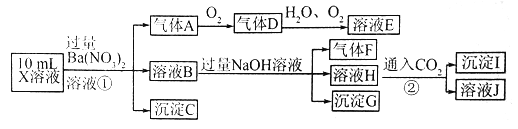
A. X 中肯定存在 Fe2+、A13+、NH4+、SO42-
B. X中不能确定是否存在的离子是Al3+和Cl-
C. 溶液E和气体F发生反应,生成物为盐类
D. 气体A是NO
【答案】A
【解析】在强酸性溶液中不可能存在大量的弱酸根离子CO32ˉ、SO32ˉ;向该溶液中加入过量Ba(NO3)2溶液,产生气体A和沉淀,说明在该溶液中含有还原性微粒Fe2+,反应产生的气体A是NO,NO与O2发生反应产生D是NO2,NO2与H2O、O2发生反应形成E是HNO3,沉淀C是BaSO4;向溶液B中加入过量NaOH溶液,发生反应产生气体F是NH3,说明在原溶液中含有NH4+;产生沉淀G是Fe(OH)3;向得到的溶液H中通入CO2气体,产生沉淀I,沉淀可能是氢氧化铝或碳酸钡,因此不能说明在该H中含有AlO2-,则在原溶液中不一定含有A13+。综上所述可知在原溶液中含有Fe2+、SO42ˉ、NH4+;不含有的离子是CO32ˉ、SO32ˉ,不能确定的离子是Al3+、Cl-。A.X中肯定存在Fe2+、NH4+、SO42ˉ,A错误;B. 根据以上分析可知X中不能确定是否存在的离子是Al3+和Cl-,B正确;C.在E中含有HNO3,气体F是NH3,二者会发生反应:HNO3+NH3=NH4NO3,硝酸铵是盐,C正确;D.根据上述分析可知气体A是NO,D正确;答案选A。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ① | |||||||
二 | ② | ③ | ④ | |||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在标号元素中,最活泼的金属元素是____。最活泼的非金属元素是____。(写元素符号)⑨元素的离子结构示意图是____________________。
(2)①与②形成共价化合物的电子式 _______________。用电子式表示⑤与⑨形成化合物的形成过程__________________________________________。
(3)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是________。(写元素符号)
(4)⑦、⑧、⑨三种元素所形成的气态氢化物中,最稳定的氢化物是____(写分子式);其三种元素的最高价含氧酸的酸性由强到弱的顺序 _________。(写酸的分子式)
(5)写出⑥元素的单质与氢氧化钠反应的离子方程式:____________________。
【题目】图中UZ六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )
序号 | U | W | Y | X |
|
① | Na | H2O | Na2O2 | NaOH | |
② | Fe | H2O | C | H2 | |
③ | HBr | Cl2 | CH4 | HCl | |
④ | CuCl2(aq) | Al | HCl(aq) | AlCl3(aq) |
A. ②④ B. ②③ C. ①②④ D. ①②③④
【题目】1 L某待测液中除含有0.2mol L的Na+外,还可能含有下列离子中的一种或多种:
阳离子 | K+、NH4+、Fe3+、Ba2+ |
阴离子 | Cl-、Br-、CO32-、HCO3-、SO32-、SO42- |
现进行如下实验操作(每次实验所加试剂均过量):

已知:无色气体D为单一气体。 请回答下列问题:
(1)气体B为_________(填化学式),白色沉淀E为________________(填化学式)。
(2)待测液中肯定存在的阴离子有______________________。
(3)写出生成白色沉淀B的离子方程式:_________________________________。
(4)判断原溶液中K+是否存在,若存在,其物质的量浓度的最小值为多少;若不存在,请说明理由:_________________________________________________________。