籾朕坪否
委吉嵎楚議署奉綻蛍艶慧壓⦿〙歓剳賑(O2)嶄◉〖屈剳晒娘賑悶嶄◉〗腎賑嶄。頼畠伴付朔⇧誼欺議耕悶麗嵎議嵎楚蛍艶斤哘議頁w1g⇧w2g才w3g。參貧眉宀議購狼屎鳩議頁
A⤴w1﹅w2﹅w3 B⤴w3﹅w1﹅w2
C⤴w3﹅w2﹅w1 D⤴w2﹅w1﹅w3
‐基宛/
D
‐盾裂/綻壓剳賑⇧腎賑賜屈剳晒娘嶄伴付郡哘議晒僥圭殻塀慌嗤⦿
2Mg+O2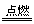 2MgO 3Mg+N2
2MgO 3Mg+N2 Mg3N2
2Mg+CO2
Mg3N2
2Mg+CO2 3MgO+C
3MgO+C
喇噐綻壓剳賑嶄伴付峪伏撹MgO⇧遇綻壓屈剳晒娘賑悶嶄伴付伏撹MgO才C◉侭參W2﹅W1。遇綻壓腎賑嶄伴付⇧茅伏撹MgO翌⇧珊嗤富楚Mg3N2。
譜1mol綻頼畠嚥O2郡哘伏撹1molMgO⇧凪耕悶嵎楚葎40g◉1molMg嚥紀賑頼畠郡哘⇧伏撹1/3molMg3N2。耕悶嵎楚葎33.3g⇧絞籾嶄伏撹議耕悶嵎楚哘壓40g嚥33.3g岻寂。侭參嗤W1﹅W3。忝栽貧峰蛍裂⇧誼購狼塀葎W2﹅W1﹅W3。

膳楼過狼双基宛
屢購籾朕
委吉嵎楚議署奉綻蛍艶慧壓↙1⇄剳賑⇧↙2⇄腎賑⇧↙3⇄屈剳晒娘賑悶嶄頼畠伴付⇧誼欺議耕悶嵎楚蛍艶頁W1、W2、W3⇧眉宀議寄弌購狼頁↙ ⇄
| A、W1﹅W2﹅W3 | B、W1=W2=W3 | C、W3﹅W1﹅W2 | D、W3﹅W2﹅W1 |