题目内容
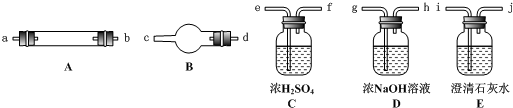
水蒸气通过灼热的焦炭后,流出气体的主要成分是CO和H2,还有CO2和水蒸气等.请用下图中提供的仪器,选择必要的试剂,设计一个实验,证明上述混合气体中有CO和H2.(加热装置和导管等在图中略去)
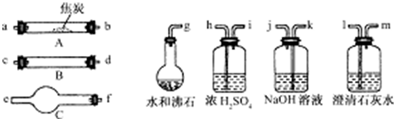
回答下列问题:
(1)盛浓H2SO4的装置用途是 ,盛NaOH溶液的装置用途是 .
(2)仪器B中需加入试剂的名称(或化学式)是 ,所发生反应的化学方程式是 .
(3)仪器C中需加入试剂的名称(或化学式)是 ,其目的是 .
(4)按气流方向连接各仪器,用字母表示接口的连接顺序:g-ab- .
(5)能证明混合气体中含有CO的实验依据是 .
(6)能证明混合气体中含有H2的实验依据是 .

回答下列问题:
(1)盛浓H2SO4的装置用途是
(2)仪器B中需加入试剂的名称(或化学式)是
(3)仪器C中需加入试剂的名称(或化学式)是
(4)按气流方向连接各仪器,用字母表示接口的连接顺序:g-ab-
(5)能证明混合气体中含有CO的实验依据是
(6)能证明混合气体中含有H2的实验依据是
分析:本题关键是应明确实验目的(证明混合气体中有CO和H2),要想达到目的,只能利用它们的还原性将之转化为CO2和H2O来检验,同时又要防止原混合气体中CO2和水蒸气的干扰,所以,用CO、H2还原CuO之前,必须首先除去CO2和水蒸气,装置连接顺序为g-ab-kj-hi-cd-fe-lm;
(1)浓硫酸是干燥气体除去水蒸气的作用;
(2)仪器B是把氢气和一氧化碳转化为水蒸气和二氧化碳进行实验验证的试剂,应选择氧化铜,氧化铜被氢气、一氧化碳氧化为水和二氧化碳;
(3)装置C中是检验生成的气体中是否含水,来证明原气体中含有氢气,选择无水硫酸铜,遇水变蓝色;
(4)证明混合气体中有CO和H2,要想达到目的,只能利用它们的还原性将之转化为CO2和H2O来检验,同时又要防止原混合气体中CO2和水蒸气的干扰,所以,用CO、H2还原CuO之前,必须首先除去CO2和水蒸气;
(5)原混合气体中二氧化碳除净后,通过氧化铜又生成二氧化碳气体,使澄清石灰水变浑浊证明存在一氧化碳;
(6)除去原混合气体中水蒸气,通过氧化铜又生成水蒸气,使白色的无水硫酸铜变蓝证明含有氢气.
(1)浓硫酸是干燥气体除去水蒸气的作用;
(2)仪器B是把氢气和一氧化碳转化为水蒸气和二氧化碳进行实验验证的试剂,应选择氧化铜,氧化铜被氢气、一氧化碳氧化为水和二氧化碳;
(3)装置C中是检验生成的气体中是否含水,来证明原气体中含有氢气,选择无水硫酸铜,遇水变蓝色;
(4)证明混合气体中有CO和H2,要想达到目的,只能利用它们的还原性将之转化为CO2和H2O来检验,同时又要防止原混合气体中CO2和水蒸气的干扰,所以,用CO、H2还原CuO之前,必须首先除去CO2和水蒸气;
(5)原混合气体中二氧化碳除净后,通过氧化铜又生成二氧化碳气体,使澄清石灰水变浑浊证明存在一氧化碳;
(6)除去原混合气体中水蒸气,通过氧化铜又生成水蒸气,使白色的无水硫酸铜变蓝证明含有氢气.
解答:解:(1)浓硫酸可以做干燥剂,盛浓H2SO4的装置用途是将气体干燥,除去水蒸气,检验一氧化碳还原氧化铜的产物二氧化碳之前要先将生成的二氧化碳除去,可以用氢氧化钠来吸收,
故答案为:除去水蒸气;除去CO2;
(2)检验合气体中有CO和H2可用氧化铜,发生反应:CuO+H2
Cu+H2O、CuO+CO
Cu+CO2,氢气和一氧化碳还原氧化铜是在大试管中进行的;
故答案为:氧化铜(CuO);CuO+H2
Cu+H2O、CuO+CO
Cu+CO2;
(3)检验水可用无水硫酸铜,将其装入干燥管中进行检验,
故答案为:无水硫酸铜(CuSO4);检验H2O;
(4)为了验证混合气中含有CO和H2,实验仪器的连接先后顺序为:除二氧化碳→除掉水分→还原装置→检验水分→检验二氧化碳;除杂质连接仪器的原则是:长进短出;
故答案为:kj-hi-cd(或dc)-fe-lm;
(5)如果有CO存在,CO和黑色的氧化铜反应生成红色的铜和二氧化碳,原混合气中的CO2已被除去,其中CO与CuO反应生成的CO2使澄清石灰水变浑浊;
故答案为:原混合气体中的CO2已被除去,B中黑色的CuO变成红色粉末,最后装置的澄清石灰水变浑浊;
(6)如果有氢气存在,氢气和黑色的氧化铜反应生成红色的铜和水,水和白色的无水硫酸铜反应生成蓝色的硫酸铜晶体,
故答案为:原混合气体中的H2O已被除去,B中黑色的CuO变成红色粉末,C中无水硫酸铜由白色变为蓝色.
故答案为:除去水蒸气;除去CO2;
(2)检验合气体中有CO和H2可用氧化铜,发生反应:CuO+H2
| ||
| ||
故答案为:氧化铜(CuO);CuO+H2
| ||
| ||
(3)检验水可用无水硫酸铜,将其装入干燥管中进行检验,
故答案为:无水硫酸铜(CuSO4);检验H2O;
(4)为了验证混合气中含有CO和H2,实验仪器的连接先后顺序为:除二氧化碳→除掉水分→还原装置→检验水分→检验二氧化碳;除杂质连接仪器的原则是:长进短出;
故答案为:kj-hi-cd(或dc)-fe-lm;
(5)如果有CO存在,CO和黑色的氧化铜反应生成红色的铜和二氧化碳,原混合气中的CO2已被除去,其中CO与CuO反应生成的CO2使澄清石灰水变浑浊;
故答案为:原混合气体中的CO2已被除去,B中黑色的CuO变成红色粉末,最后装置的澄清石灰水变浑浊;
(6)如果有氢气存在,氢气和黑色的氧化铜反应生成红色的铜和水,水和白色的无水硫酸铜反应生成蓝色的硫酸铜晶体,
故答案为:原混合气体中的H2O已被除去,B中黑色的CuO变成红色粉末,C中无水硫酸铜由白色变为蓝色.
点评:本题考查了物质性质的实验设计和实验验证的方法应用,回答本题要知道除杂质时要把水放到最后除去,如果验证水的存在时要把验证水存在的无水硫酸铜放在最前面.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目