题目内容
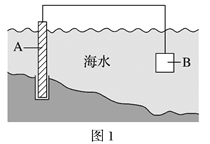
【题目】海洋中有丰富的资源,下图为海水利用的部分过程。下列有关说法正确的是

A. 由反应①可知:相同温度下,NaHCO3的溶解度大于Na2CO3
B. 通过电解MgCl2·6H2O晶体可以获得Mg单质
C. 反应②的离子方程式为:Br2+SO2+2H2O=SO42-+2Br—+4H+
D. 粗盐中含有的Mg2+、SO42-等杂质离子,可通过依次加入BaCl2溶液、NaOH溶液、盐酸等试剂加以去除
【答案】C
【解析】
A.往NaCl溶液中通氨气、二氧化碳,得到的沉淀是NaHCO3,说明碳酸氢钠的溶解度小于氯化钠,此过程不能判断NaHCO3的溶解度大于Na2CO3,事实上碳酸钠的溶解度大于碳酸氢钠,故A错误;
B.镁是活泼的金属,工业上通过电解熔融的氯化镁得到金属镁,故B错误;
C.反应②中二氧化硫溶液与单质溴反应生成硫酸和HBr,反应的离子方程式为Br2+SO2+2H2O=SO42-+2Br—+4H+,故C正确;
D.粗盐中含有的Mg2+、SO42-等杂质离子,先转化为沉淀,可通过依次加入BaCl2溶液、NaOH溶液、盐酸,但是过量的BaCl2溶液无法除去,应该加入氯化钡、氢氧化钠、碳酸钠,过滤后在加入盐酸,故D错误。
故答案选C。

【题目】化学反应是化学实验现象的本质,根据描述回答下列问题:
(1)在BaCl2溶液中通入SO2气体,未见沉淀生成,若先通入或加入下列的另一种物质,再通入SO2不能看到沉淀的有 (填序号).
①Cl2②NaOH③HCl④FeCl3溶液⑤CO2⑥H2S⑦NH3⑧NaClO溶液
(2)图中A、B、C之间有以下的转化关系(副产物已略去);
![]()
则下列说法正确的是
a.若A是非金属单质,则C与水反应的生成物可能是强酸或弱酸
b.若A是金属单质,则C与水反应的生成物可能是强碱
c.若A是化合物,则C与水反应的生成物可能是强酸
(3)离子方程式是重要的化学用语.下列是有关离子方程式的一些错误观点,请在下列表格相应的“离子方程式”否定这些观点.
反应物从下列物质中选取:Na、Fe、H2O、H2SO4、HCl、NaOH、Ba(OH)2、CuSO4
错误观点 | “否定的”离子方程式 | |
① | 所有的离子方程式均可以表示一类化学反应 |
|
② | 所有酸碱中和反应均可表示为 H++OH﹣═H2O |
|