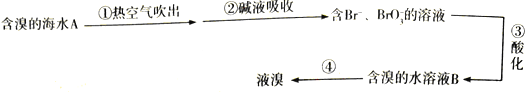
题目内容
【题目】某烯烃A,分子式为C8H16,A在一定条件下被氧化只生成一种物质B,B能与纯碱反应。已知:
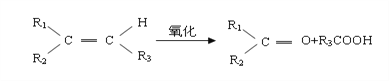
则符合上述条件的烃A有 ( ) 种(不考虑顺反异构)。
A. 2 B. 3 C. 4 D. 5
【答案】A
【解析】某烯烃A,分子式为C8H16,A在一定条件下被氧化只生成一种物质B,说明分子是对称的,结构简式为(不考虑顺反异构):CH3CH2CH2CH=CHCH2CH2CH3、(CH3)2CHCH=CHCH(CH3)2、CH3CH2(CH3)C=C(CH3)CH2CH3,根据已知中的氧化规律,双键碳上连1个氢原子时氧化为羧酸,双键碳上没有氢原子时氧化为酮,又因为B能与纯碱反应,所以B应为羧酸,因此只有CH3CH2CH2CH=CHCH2CH2CH3和(CH3)2CHCH=CHCH(CH3)2氧化产物符合题意,故选A。

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案【题目】硅酸盐在地壳中分布很广,可用蛭石生产硫酸镁和氢氧化镁。某地蛭石的主要成分是[(Mg2.36Fe0.48Al0.16)(Si2.72Al1.28)O10(OH)2] ·[Mg0.32(H2O)0.42],还含有少量杂质FeO。
实验步骤如下:
Ⅰ.制取粗硫酸镁:用硫酸浸泡蛭石矿粉,过滤,将滤液结晶得到粗硫酸镁。
Ⅱ.提纯粗硫酸镁:将粗硫酸镁在酸性条件下溶解,加入适量的0.1mol·L—1H2O2溶液,再加试剂A调节溶液pH,并分离提纯。
Ⅲ.制取氢氧化镁:向步骤Ⅱ得的溶液中加入过量氨水。
一些金属离子转化为氢氧化物沉淀时溶液的pH如表1所示
表1
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
完全沉淀时 | 3.7 | 5.2 | 9.7 |
请回答:
(1)在步骤Ⅱ中加H2O2溶液的目的是___________。调节溶液pH的范围是______________。试剂A的最佳选择是_________(填字母序号)。
A、MgO B、Na2CO3 C、蒸馏水 D、稀硫酸
(2)测定粗硫酸镁中Fe2+的含量。称取12.3g粗硫酸镁样品溶于水形成溶液,完全转移到锥形瓶中,加稀硫酸酸化,滴加几滴黄色铁氰化钾K3[Fe(CN)6]溶液,用0.010 mol·L—1H2O2溶液进行滴定。平行测定4组,消耗H2O2溶液的体积数据记录如表2所示。
表2
实验编号 | 1 | 2 | 3 | 4 | 平均值 |
消耗H2O2溶液的体积/mL | 12.49 | 12.50 | 13.62 | 12.51 |
①K3[Fe(CN)6]与Fe2+反应生成带有特征蓝色的铁氰化亚铁沉淀,请写出反应的离子方程:________。
②反应达到终点时的标志是_________________________________________________。
③根据表2数据,可计算出粗硫酸镁样品中含有Fe2+_______________mol。
(3)工业上常以Mg2+的转化率为考查指标来确定步骤Ⅲ制备氢氧化镁工艺过程的适宜条件。
①步骤Ⅲ中制备氢氧化镁反应的离子方程式为_________________________。
②已知25℃时,Mg(OH)2和Ca(OH)2的Ksp分别为2×10-11和4.7×10—6。若用石灰乳替代氨水,__________(填“能”或“不能”)制氢氧化镁,理由是_____________________________。
③通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,Mg2+完全沉淀时溶液的pH为________。(保留小数点后一位)(已知lg2=0.3)