题目内容
【题目】七铝十二钙是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:
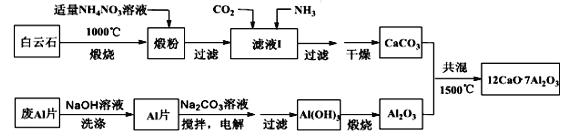
(1)煅粉主要含__________,该工艺中不能用(NH4)2SO4代替NH4NO3,原因是_________。
(2)滤液I中主要的阴离子有_________;若滤液I中仅通入CO2,会生成________,从而导致CaCO3产率降低。
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为______________。
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式为_______________。
【答案】CaO,MgO加入(NH4)2SO4会生成CaSO4微溶物,在过滤时会被除去,造成生成的CaCO3减少NO3-、OH-Ca(HCO3)22OH-+Al2O3=2AlO2-+H2O2Al+6H2O![]() 2Al(OH)3↓+3H2↑
2Al(OH)3↓+3H2↑
【解析】
(1)白云石煅烧CaCO3 ·MgCO 3 ![]() CaO·MgO+2CO2 ↑,煅粉主要含 CaO,MgO ,用(NH4)2SO4代替NH4NO3,会生成CaSO4沉淀,引起Ca2+ 的损失;答案: (1). CaO,MgO (2). 加入(NH4)2SO4会生成CaSO4微溶物,在过滤时会被除去,造成生成的CaCO3减少
CaO·MgO+2CO2 ↑,煅粉主要含 CaO,MgO ,用(NH4)2SO4代替NH4NO3,会生成CaSO4沉淀,引起Ca2+ 的损失;答案: (1). CaO,MgO (2). 加入(NH4)2SO4会生成CaSO4微溶物,在过滤时会被除去,造成生成的CaCO3减少
(2)煅粉中加入NH4NO3,NH4+ 水解后呈酸性,CaO溶解生成Ca(NO3)2 和NH3·H2O,过滤后溶液中含有Ca(NO3)2 和NH3·H2O,通入CO2和NH3后发生Ca(NO3)2+2NH3+CO2+H2O=CaCO3+2NH4NO3,故溶液主要的阴离子有 NO3-、OH-,仅通入CO2会发生CaCO3+H2O+2CO2=Ca(HCO3)2 ,从而导致CaCO3产率过低。答案: (3). NO3-、OH- (4). Ca(HCO3)2 。息分利用题目拨给
(3)铝的氧化膜就是氧化铝,具有两性,能溶于碱Al2O3 + 2NaOH = 2NaAlO2 + H2O,反应的离子方程式为 2OH-+Al2O3=2AlO2-+H2O ,答案: (5). 2OH-+Al2O3=2AlO2-+H2O
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,Al作阳极,石墨作阴极,Al在阳极放电,溶液中的H+在阴极放电,破坏了水的电离平衡,使得溶液中的OH-浓度增大,与产生的Al3+结合生成Al(OH)3,总反应方程式为2Al+6H2O![]() 2Al(OH)3↓+3H2↑,答案:(6). 2Al+6H2O
2Al(OH)3↓+3H2↑,答案:(6). 2Al+6H2O![]() 2Al(OH)3↓+3H2↑
2Al(OH)3↓+3H2↑

【题目】甲、乙、丙、丁均为中学化学常见的纯净物,它们之间有如图所示的反应关系。下列物质组不满足上述转化关系的是
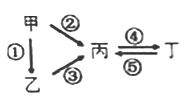
选项 | 甲 | 乙 | 丙 | 丁 |
A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
B | S | H2S | SO3 | H2SO4 |
C | N2 | NH3 | NO | NO2 |
D | Si | SiO2 | Na2SiO3 | Na2CO3 |
A. A B. B C. C D. D