题目内容
将2.0mol/L CuSO4溶液和1.0mol/L H2SO4 溶液等体积混合.计算:
(1)混合液中CuSO4和H2SO4的物质的量浓度;
(2)混合液中H+、SO42-的物质的量浓度.(可认为体积具有加和性)
解:设体积都为VL,则
n( CuSO4)=2Vmol;n(H2SO4)=VmoL;n(H+)=2n(H2SO4)=2VmoL;n(SO42-)=n( CuSO4)+n(H2SO4)=2Vmol+Vmol=3Vmol.
(1)c(CuSO4)= =1.0mol/L,c(H2SO4)=
=1.0mol/L,c(H2SO4)=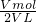 =0.5mol/L.
=0.5mol/L.
答:CuSO4的物质的量浓度为1.0 mol/L,H2SO4的物质的量浓度为0.5 mol/L;
(2)c(H+)= =1mol/L,c(SO42-)=
=1mol/L,c(SO42-)= =1.5mol/L.
=1.5mol/L.
答:H+的物质的量浓度为1.0 mol/L、SO42-的物质的量浓度为1.5 mol/L.
分析:根据体积和物质的量浓度可以计算各粒子的物质的量,用c= 结合溶液混合前后溶质的物质的量不变计算溶液中各粒子的物质的量浓度.
结合溶液混合前后溶质的物质的量不变计算溶液中各粒子的物质的量浓度.
点评:本题考查物质的量浓度的相关计算,题目难度不大,注意相关计算公式的运用.
n( CuSO4)=2Vmol;n(H2SO4)=VmoL;n(H+)=2n(H2SO4)=2VmoL;n(SO42-)=n( CuSO4)+n(H2SO4)=2Vmol+Vmol=3Vmol.
(1)c(CuSO4)=
 =1.0mol/L,c(H2SO4)=
=1.0mol/L,c(H2SO4)=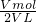 =0.5mol/L.
=0.5mol/L.答:CuSO4的物质的量浓度为1.0 mol/L,H2SO4的物质的量浓度为0.5 mol/L;
(2)c(H+)=
 =1mol/L,c(SO42-)=
=1mol/L,c(SO42-)= =1.5mol/L.
=1.5mol/L.答:H+的物质的量浓度为1.0 mol/L、SO42-的物质的量浓度为1.5 mol/L.
分析:根据体积和物质的量浓度可以计算各粒子的物质的量,用c=
 结合溶液混合前后溶质的物质的量不变计算溶液中各粒子的物质的量浓度.
结合溶液混合前后溶质的物质的量不变计算溶液中各粒子的物质的量浓度.点评:本题考查物质的量浓度的相关计算,题目难度不大,注意相关计算公式的运用.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目