题目内容
下列实验操作,正确的是( )
①除去Fe粉中混有的I2:加热使I2升华
②配制一定物质的量浓度的溶液时,将称量好的溶质溶于盛有适量水的烧杯中,待溶解后立即倾入容量瓶中,继续进行洗涤和定容③用NaOH溶液和可溶性铝盐溶液大量制取Al(OH)3④制取Fe(OH)2时,吸取除去氧气的NaOH溶液的胶头滴管的末端插入FeSO4溶液中,再逐渐注入NaOH溶液 ⑤制取氯气时,先加热再从分液漏斗滴加浓盐酸.
①除去Fe粉中混有的I2:加热使I2升华
②配制一定物质的量浓度的溶液时,将称量好的溶质溶于盛有适量水的烧杯中,待溶解后立即倾入容量瓶中,继续进行洗涤和定容③用NaOH溶液和可溶性铝盐溶液大量制取Al(OH)3④制取Fe(OH)2时,吸取除去氧气的NaOH溶液的胶头滴管的末端插入FeSO4溶液中,再逐渐注入NaOH溶液 ⑤制取氯气时,先加热再从分液漏斗滴加浓盐酸.
分析:①加热碘与铁反应生成碘化亚铁;
②物质溶于水会有热效应,不恢复都室温,就进行溶液的定容,影响所配溶液的体积,进而影响所配溶液的浓度;
③氢氧化钠比氢氧化铝要贵,不适合用NaOH溶液和可溶性铝盐溶液大量制取Al(OH)3,且氢氧化钠过量会溶解氢氧化铝;
④氢氧化亚铁不稳定,易被氧化,制取Fe(OH)2时,为防止尽可能的少接触空气,应吸取除去氧气的NaOH溶液的胶头滴管的末端插入FeSO4溶液中,再逐渐注入NaOH溶液;
⑤制取氯气时,先从分液漏斗滴加浓盐酸再加热.
②物质溶于水会有热效应,不恢复都室温,就进行溶液的定容,影响所配溶液的体积,进而影响所配溶液的浓度;
③氢氧化钠比氢氧化铝要贵,不适合用NaOH溶液和可溶性铝盐溶液大量制取Al(OH)3,且氢氧化钠过量会溶解氢氧化铝;
④氢氧化亚铁不稳定,易被氧化,制取Fe(OH)2时,为防止尽可能的少接触空气,应吸取除去氧气的NaOH溶液的胶头滴管的末端插入FeSO4溶液中,再逐渐注入NaOH溶液;
⑤制取氯气时,先从分液漏斗滴加浓盐酸再加热.
解答:解:①加热碘与铁反应生成碘化亚铁,不能除去Fe粉中混有的I2,故错误;
②物质溶于水会有热效应,不恢复都室温,就进行溶液的定容,影响所配溶液的体积,进而影响所配溶液的浓度,应先恢复到室温,再进行定容,故错误;
③氢氧化钠比氢氧化铝要贵,不适合用NaOH溶液和可溶性铝盐溶液大量制取Al(OH)3,且氢氧化钠过量会溶解氢氧化铝,故错误;
④氢氧化亚铁不稳定,易被氧化,制取Fe(OH)2时,为防止尽可能的少接触空气,应吸取除去氧气的NaOH溶液的胶头滴管的末端插入FeSO4溶液中,再逐渐注入NaOH溶液,故正确;
⑤制取氯气时,先从分液漏斗滴加浓盐酸再加热,故错误.
故选C.
②物质溶于水会有热效应,不恢复都室温,就进行溶液的定容,影响所配溶液的体积,进而影响所配溶液的浓度,应先恢复到室温,再进行定容,故错误;
③氢氧化钠比氢氧化铝要贵,不适合用NaOH溶液和可溶性铝盐溶液大量制取Al(OH)3,且氢氧化钠过量会溶解氢氧化铝,故错误;
④氢氧化亚铁不稳定,易被氧化,制取Fe(OH)2时,为防止尽可能的少接触空气,应吸取除去氧气的NaOH溶液的胶头滴管的末端插入FeSO4溶液中,再逐渐注入NaOH溶液,故正确;
⑤制取氯气时,先从分液漏斗滴加浓盐酸再加热,故错误.
故选C.
点评:本题考查物质的分离提纯、溶液配制、物质的制备等,难度中等,掌握物质的性质与原理是关键.

练习册系列答案
相关题目
下列实验操作完全正确的是( )
|
下列实验操作完全正确的是( )
|
下列实验操作不正确的是( )
A、 定容 | B、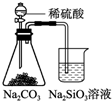 比较硫、碳、硅三种元素的非金属性强弱 | C、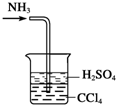 处理尾气 | D、 测定黄铜(Cu、Zn合金) 中Zn的含量 |
下列实验操作中正确的是( )
| A、配制480mL溶液需要用到500mL容量瓶 | B、用酒精萃取碘水中的碘 | C、将NaOH 固体放在托盘天平右盘的纸上称量 | D、蒸馏时应将温度计水银球插入液体中 |