题目内容
 A、B是中学化学里常见的物质,其中B是单质,A是化合物.
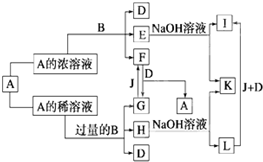
A、B是中学化学里常见的物质,其中B是单质,A是化合物.已知:往E溶液中滴加KSCN溶液时,溶液呈红色; A的浓溶液与B在常温下无明显反应现象.请回答:
(1)框图中B和A的浓溶液反应的条件是
加热
加热
,而常温下无明显现象的原因是常温下,铁遇浓硝酸发生钝化
常温下,铁遇浓硝酸发生钝化
;(2)写出F和G相互转化的化学方程式:
F→G:
3NO2+H2O═2HNO3+NO
3NO2+H2O═2HNO3+NO
;G→F:
2NO+O2=2NO2
2NO+O2=2NO2
.(3)L转化成I的化学方程式是
4Fe(OH)2+O2+2H2O═4Fe(OH)3
4Fe(OH)2+O2+2H2O═4Fe(OH)3
.分析:往E溶液中滴加KSCN溶液时,溶液呈红色,说明含有铁离子,A的浓溶液与B在常温下无明显反应现象,所以A是硝酸,B是铁,铁和浓硝酸反应生成硝酸铁、NO2和水,和稀硝酸反应生成硝酸亚铁、NO和水,因此E是硝酸铁,D是水,F是NO2,G是NO,H是硝酸亚铁,J是氧气.I是氢氧化铁,K是硝酸钠,L是氢氧化亚铁,结合对应物质的性质以及题目要求解答该题.
解答:解:往E溶液中滴加KSCN溶液时,溶液呈红色,说明含有铁离子,A的浓溶液与B在常温下无明显反应现象,所以A是硝酸,B是铁,铁和浓硝酸反应生成硝酸铁、NO2和水,和稀硝酸反应生成硝酸亚铁、NO和水,因此E是硝酸铁,D是水,F是NO2,G是NO,H是硝酸亚铁,J是氧气.I是氢氧化铁,K是硝酸钠,L是氢氧化亚铁,
(1)铁和浓硝酸在常温下发生钝化反应,在铁表面生成一层致密的氧化铁膜而阻碍反应的继续进行,则浓硝酸应与铁在加热条件下反应,
故答案为:加热;常温下,铁遇浓硝酸发生钝化;
(2)F是NO2,G是NO,NO2可与水反应生成NO,反应的化学方程式为3NO2+H2O═2HNO3+NO,NO可与氧气反应生成NO2,反应的方程式为2NO+O2═2NO2,
故答案为:3NO2+H2O═2HNO3+NO;2NO+O2═2NO2;
(3)L为Fe(OH)2,可与氧气、水反应生成Fe(OH)3,反应的方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3.
(1)铁和浓硝酸在常温下发生钝化反应,在铁表面生成一层致密的氧化铁膜而阻碍反应的继续进行,则浓硝酸应与铁在加热条件下反应,
故答案为:加热;常温下,铁遇浓硝酸发生钝化;
(2)F是NO2,G是NO,NO2可与水反应生成NO,反应的化学方程式为3NO2+H2O═2HNO3+NO,NO可与氧气反应生成NO2,反应的方程式为2NO+O2═2NO2,
故答案为:3NO2+H2O═2HNO3+NO;2NO+O2═2NO2;
(3)L为Fe(OH)2,可与氧气、水反应生成Fe(OH)3,反应的方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3.
点评:本题考查无机物的推断,为高考常见题型,难度中等,化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合.它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法.解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目




