��Ŀ����
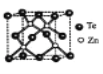
����Ŀ��(1)ij�л�����C��H��O����Ԫ����ɣ����ģ����ͼ��ʾ��
�ٺ��еĹ�����������_______��
��д�����л���������Ʒ�Ӧ�Ļ�ѧ����ʽ_______��
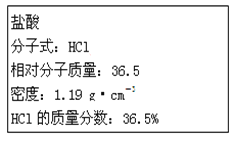
(2)���ֳ����л�����ӵı���ģ��ʾ��ͼ���£����мס��ҡ���Ϊ������Ϊ���������

�ٿ��Լ�����ҵ��Լ�Ϊ_________��
a.ϡ���� b.������Ȼ�̼��Һ c.ˮ d.���Ը��������Һ
�������������ж�����������ζ���Ҳ�����ˮ���ܶȱ�ˮС����_________�������ƣ���
���ҺͶ������ʵ�����1.5mol����ȫȼ����Ҫ�����������ʵ�����_______��
���𰸡�̼̼˫�����Ȼ� 2CH2=CH-COOH+2Na��2CH2=CH- COONa+H2�� bd �� 4.5mol
��������
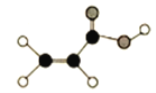
(1)���ݼۼ����ɺ����ģ����д���л���Ľṹ��ʽCH2=CHCOOH���ݴ�д�����������������ƣ����л��ﺬ���Ȼ����ܹ����Ʒ�Ӧ�ų��������ݴ�д������ʽ��
(2)����������Ϊ��������Ϊ�������������ݱ���ģ�Ϳ�֪�����л�������Ϊ���顢��Ϊ��ϩ����Ϊ������Ϊ�Ҵ������������ʵ�������ʽ��з������
(1)�����ݼۼ����ɺ����ģ�������л���Ľṹ��ʽΪ��CH2=CHCOOH�����еĹ�����Ϊ̼̼˫�����Ȼ����������������������̼̼˫�����Ȼ���
��CH2=CHCOOH���Ʒ�Ӧ���������κ���������ѧ����ʽΪ��2CH2=CH-COOH+2Na��2CH2=CH-COONa+H2�����������������������2CH2=CH-COOH+2Na��2CH2=CH-COONa+H2����
(2)�ɱ���ģ�Ϳ�֪��Ϊ���顢��Ϊ��ϩ����Ϊ������Ϊ�Ҵ���
��a��������ϩ������ϡ���ᷴӦ��Ҳ������ˮ�������𣬹ʲ�ѡa�
b���ϩ����������Ȼ�̼��Һ�����ӳɷ�Ӧ��ʹ����ɫ�����鲻��ʹ������Ȼ�̼��Һ��ɫ���ʿ��Լ��𣬹�ѡb�
c��������ϩ��������ˮ���������𣬹ʲ�ѡc�
d���ϩ��̼̼˫�������Ա����Ը������������ʹ���Ը��������Һ��ɫ�����鲻�ܱ����Ը��������Һ��������ѡd�
��������������ѡbd��
���ж�����������ζ���Ҳ�����ˮ���ܶȱ�ˮС���л���Ϊ������Ϊ���õ��л��ܼ�������������������ǣ�����
����Ϊ��ϩ����Ϊ�Ҵ���1.5mol��ϩ��ȫȼ����Ҫ���������ʵ�����1.5����2+4/4��=4.5mol��1.5mol�Ҵ���ȫȼ����Ҫ�����������ʵ�����1.5����2+6/4-1/2��=4.5mol������1.5mol��ϩ���Ҵ��Ļ��������ȫȼ����Ҫ�����������ʵ�����4.5mol���������������������4.5mol��

����Ŀ�����ǻ�ѧʵ���Ҽ����������е���Ҫ���ʣ�Ӧ�ù㷺��
(1)��֪25��ʱ��N2��g��+O2��g��![]() 2NO��g�� ��H1��+183kJ��mol
2NO��g�� ��H1��+183kJ��mol
2H2��g��+O2��g����2H2O��1�� ��H2��-571.6kJ��mol
4NH3��g��+5O2��g����4NO��g��+6H2O��1�� ��H3��-1164.4kJ��mol
��N2��g��+3H2��g��![]() 2NH3��g�� ��H��________kJ��mol
2NH3��g�� ��H��________kJ��mol
(2)�ں��º����ܱ������н��кϳɰ���Ӧ����ʼͶ��ʱ������Ũ�����±���
N2 | H2 | NH3 | |
Ͷ��I | 1.0mol/L | 3.0mol/L | 0 |
Ͷ��II | 0.5mol/L | 1.5mol/L | 1.0mol/L |
�ٰ�Ͷ��I���з�Ӧ����ôﵽ��ѧƽ��״̬ʱH2��ת����Ϊ40��������Ͷ��II���з�Ӧ����ʼʱ��Ӧ���еķ���Ϊ________��������������������������
��L��L1��L2����X�ɷֱ����ѹǿ���¶ȡ���ͼ��ʾLһ��ʱ���ϳɰ���Ӧ��H2��g����ƽ��ת������X
�ı仯��ϵ��
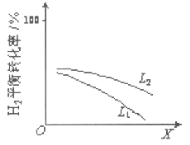
iX��������������_________��
ii�ж�L1��L2�Ĵ�С��ϵ�����������ɣ�_____________��
����Ŀ�����и��鷴Ӧ(�������ʾ�Ϊ��Ӧ��)�տ�ʼʱ���ų�H2������������
��� | ����(��ĩ״) | ���Ũ�� | ������ | ��Ӧ�¶� |
A | 0.1mol Mg | 6mol/L���� | 10mL | 30�� |
B | 0.1mol Mg | 3mol/L���� | 10mL | 60�� |
C | 0.1mol Fe | 3mol/L���� | 10mL | 60�� |
D | 0.1mol Mg | 3mol/L���� | 10mL | 30�� |
A. AB. BC. CD. D