题目内容
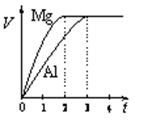
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图。关于反应中镁和铝的说法正确的是( )

| A.质量之比为3:2 |
| B.物质的量之比为2:3 |
| C.摩尔质量之比为2:3 |
| D.消耗硫酸的物质的量之比为1:1 |
D
试题分析:根据图像可知,生成的体积氢气相等。由于稀硫酸是过量的,所以根据方程式Mg+2H+=Mg2++H2↑、2Al+6H+=2Al3++3H2↑可知,镁和铝的物质的量之比是3:2,质量之比是4:3,A、B、C都是错误的。根据氢原子守恒可知,消耗的硫酸是相等的,答案选D。
点评:该题是高考中的常见题型,属于中等难度的试题。试题通过和图像相联系,增加了试题的难度,有利于培养学生的灵活应变能力。该题设计新颖,基础性强,有利于培养学生的逻辑思维能力。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
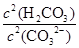 填(“变大”、“变小”或“不变”)
填(“变大”、“变小”或“不变”) 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积 溶液
溶液 过滤,测定得到沉淀的质量
过滤,测定得到沉淀的质量