题目内容
有关下列有机物在相同条件下性质比较的说法中,正确的是( )
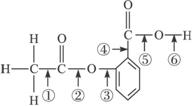
| A、乙酸乙酯在水中的溶解度比乙醇在水中的溶解度大 | B、异丁烷的沸点比正丁烷的沸点高 | C、苯酚的酸性比CH3COOH的酸性强 | D、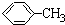 比 比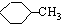 更易被KMnO4酸性溶液氧化 更易被KMnO4酸性溶液氧化 |
分析:A.乙醇与水形成氢键,溶解性强;
B.同分异构体中,支链越多,沸点越低;
C.醋酸与苯酚钠反应生成苯酚,为强酸制取弱酸的反应;
D.苯环影响甲基,使甲基易被氧化.
B.同分异构体中,支链越多,沸点越低;
C.醋酸与苯酚钠反应生成苯酚,为强酸制取弱酸的反应;
D.苯环影响甲基,使甲基易被氧化.
解答:解:A.乙醇与水形成氢键,溶解性强,则乙酸乙酯在水中的溶解度比乙醇在水中的溶解度小,故A错误;
B.同分异构体中,支链越多,沸点越低,则异丁烷的沸点比正丁烷的沸点低,故B错误;
C.醋酸与苯酚钠反应生成苯酚,为强酸制取弱酸的反应,则苯酚的酸性比CH3COOH的酸性弱,故C错误;
D.苯环影响甲基,使甲基易被氧化,则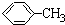 比
比 更易被KMnO4酸性溶液氧化,故D正确;
更易被KMnO4酸性溶液氧化,故D正确;
故选D.
B.同分异构体中,支链越多,沸点越低,则异丁烷的沸点比正丁烷的沸点低,故B错误;
C.醋酸与苯酚钠反应生成苯酚,为强酸制取弱酸的反应,则苯酚的酸性比CH3COOH的酸性弱,故C错误;
D.苯环影响甲基,使甲基易被氧化,则
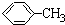 比
比 更易被KMnO4酸性溶液氧化,故D正确;
更易被KMnO4酸性溶液氧化,故D正确;故选D.
点评:本题考查有机物的结构与性质,为高频考点,涉及氢键、沸点比较、酸性比较及原子团之间相互影响等,注重规律性知识的应用和分析能力的考查,题目难度不大.

练习册系列答案
相关题目
在下列有关说法中正确的是( )
①相同质量的CH4、C2H4、C2H2完全燃烧时耗O2量的关系为CH4>C2H4>C2H2
②对于任意比混合的乙烯、丙烯混合气体在足量氧气中燃烧,只要混合气体的质量不变,完全燃烧后产生的CO2和H2O的量也不变
③对于任意比混合的C2H4、C2H6、C2H2混合气体,只要混合气体物质的量不变,完全燃烧后产生的CO2物质的量也不改变
④某有机物在足量氧气中燃烧后产生CO2与H2O的物质的量之比为2:3,则该有机物的类型肯定为烷烃.
①相同质量的CH4、C2H4、C2H2完全燃烧时耗O2量的关系为CH4>C2H4>C2H2
②对于任意比混合的乙烯、丙烯混合气体在足量氧气中燃烧,只要混合气体的质量不变,完全燃烧后产生的CO2和H2O的量也不变
③对于任意比混合的C2H4、C2H6、C2H2混合气体,只要混合气体物质的量不变,完全燃烧后产生的CO2物质的量也不改变
④某有机物在足量氧气中燃烧后产生CO2与H2O的物质的量之比为2:3,则该有机物的类型肯定为烷烃.
| A、①②③ | B、②③④ | C、①②④ | D、以上组合均不正确 |
(28分)
[1]由碳、氢、氧三种元素组成的某有机物分子中共含有13个原子,其原子核外共有40个电子,l mol该有机物在氧气中完全燃烧时需消耗5.5 mol O2。请回答:
(1)试求出该有机物的分子式为 。
(2)若该有机物可使溴水褪色,且分子中不含有甲基,也不能发生银镜反应,取0.1 m ol该有机物与足量钠反应,能产生1.12 L H2(标准状况),则该有机物的结构简式可能是 ;该有机物在一定条件下发生聚合反应的化学方程式是 。
ol该有机物与足量钠反应,能产生1.12 L H2(标准状况),则该有机物的结构简式可能是 ;该有机物在一定条件下发生聚合反应的化学方程式是 。
(3)若该有机物能发生银镜反应,且分子中只含有一个甲基,则其结构简式是 。
(4)若该有机物的结构呈环状,且既不含甲基又不含羟基,则其键线式是 。
|
|
溶成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强
的毒性。请回答下列问题:
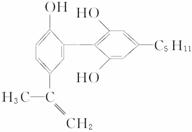
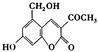
(1)“亮菌甲素”的分子式为 。
(2)丙二醇的分子式是C3H8O2,已知两个羟基连在同一个碳原子上的物质不存在。写出其属于醇类的同分异构体的结构简式 。
(3)下列有关“亮菌甲素”的叙述正确的是 (填序号)。
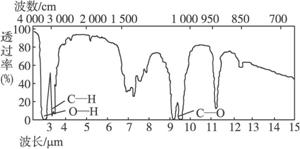
A.“亮菌甲素”能与H2发生加成反应 B.不能使酸性KMnO4退色
C.“亮菌甲素”分子中含氧官能团只有2种 D.1mol“亮菌甲素”最多与2molNaOH反应
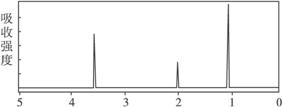
(4)核磁共振氢谱分析,发现二甘醇分子中有3个肿收峰,其峰面积之比为2:2:1。又知二甘醇中C、O元素的质量分数相同,且H的质量分数为9.4%,1mol二甘醇与足量的金属钠反应生成1molH2。写出二甘醇与乙酸(按物质的量之比1:1)反应的化学方程式

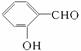 的沸点高于
的沸点高于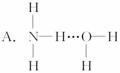


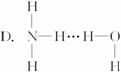
 ,它配以辅料丙二醇溶成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性。请回答下列问题:
,它配以辅料丙二醇溶成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性。请回答下列问题: