题目内容
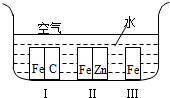 (1)如图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)
(1)如图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)(2)氟氯代烷是一种能破坏臭氧层的物质.在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:
①Cl+O3→ClO+O2 ②O3→O+O2 ③ClO+O→Cl+O2
上列的反应的总反应式是
分析:(1)金属腐蚀时,原电池腐蚀比化学腐蚀快,当铁为原电池负极时,易被氧化而腐蚀,当为原电池正极时,得到保护;
(2)将方程式①②③相加得出氧气和臭氧的关系式;根据Cl+O3→ClO+O2 判断氟氯代烷能破坏大量臭氧的原因.
(2)将方程式①②③相加得出氧气和臭氧的关系式;根据Cl+O3→ClO+O2 判断氟氯代烷能破坏大量臭氧的原因.
解答:解:(1)铁处于Ⅰ的环境中做原电池的负极,腐蚀速率较快,铁处于Ⅱ的环境中做原电池的正极,被保护,腐蚀速率很慢,铁处于Ⅲ的环境中的金属铁发生吸氧腐蚀,速度较慢,
故答案为:Ⅰ、Ⅲ、Ⅱ;
(2)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3→3O2;
氟氯代烷受紫外线的照射分解出氯原子,Cl+O3→ClO+O2,Cl对O3的分解有促进作用,所以能破坏臭氧层,
故答案为:2O3
3O2;氟氯代烷分解产生的Cl对O3的分解有促进作用.
故答案为:Ⅰ、Ⅲ、Ⅱ;
(2)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3→3O2;
氟氯代烷受紫外线的照射分解出氯原子,Cl+O3→ClO+O2,Cl对O3的分解有促进作用,所以能破坏臭氧层,
故答案为:2O3
| ||
点评:本题考查较为综合,涉及金属的腐蚀以及环境保护等知识,为高频考点,侧重于化学与生活、环境的考查,有利于培养学生的良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
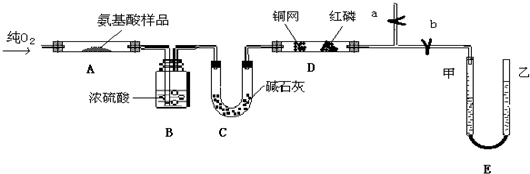
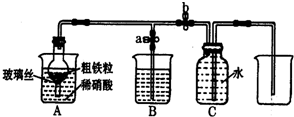 (1)如图所示是实验室中制取气体的一种简易装置.①甲同学用下列方法检验装置的气密性,请问能否达到目的
(1)如图所示是实验室中制取气体的一种简易装置.①甲同学用下列方法检验装置的气密性,请问能否达到目的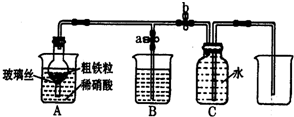 (1)如图所示是实验室中制取气体的一种简易装置.①甲同学用下列方法检验装置的气密性,请问能否达到目的______ (填能或否)
(1)如图所示是实验室中制取气体的一种简易装置.①甲同学用下列方法检验装置的气密性,请问能否达到目的______ (填能或否)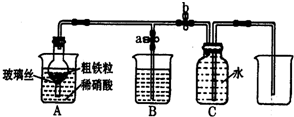
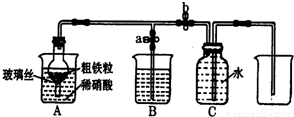 (1)如图所示是实验室中制取气体的一种简易装置.①甲同学用下列方法检验装置的气密性,请问能否达到目的 (填能或否)
(1)如图所示是实验室中制取气体的一种简易装置.①甲同学用下列方法检验装置的气密性,请问能否达到目的 (填能或否)