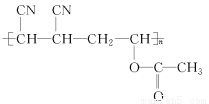
题目内容
一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为 。
②NO3-的空间构型是 (用文字描述)。
(2)在铜锰氧化物的催化下,CO被氧化为CO2,HCHO被氧化为CO2和H2O。
①根据等电子体原理,CO分子的结构式为 。
②H2O分子中O原子轨道的杂化类型为 。
③1 mol CO2中含有的σ键数目为 。
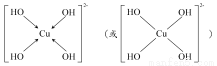
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为 。
(1)①1s22s22p63s23p63d5(或[Ar]3d5)
②平面三角形
(2)①C≡O ②sp3
③2×6.02×1023个(或2 mol)
(3)
【解析】(1)①Mn为ⅦB族元素,其基态核外电子排布式为1s22s22p63s23p63d54s2或[Ar]3d54s2,所以Mn2+的核外电子排布式为1s22s22p63s23p63d5或[Ar]3d5;②NO有3个σ键,孤对电子对数=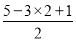 =0,所以为sp2杂化,平面三角形。
=0,所以为sp2杂化,平面三角形。
(2)①CO与N2是等电子体,N2的结构式为NN,所以CO结构式为CO;②H2O中的O原子最外层有6个电子,与两个H原子形成2个σ键,最外层还余4个电子,形成两对孤对电子,所以价层电子对数为4,sp3杂化;③1个CO2中含有2个σ键。

α、β、γ和δ四种生育三烯酚是构成维生素E的主要物质,下列叙述中不正确的是( )
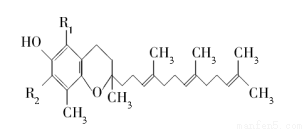
生育三烯酚
| α | β | γ | δ |
R1 | CH3 | CH3 | H | H |
R2 | CH3 | H | CH3 | H |
A.α和δ两种生育三烯酚互为同系物,β和γ两种生育三烯酚互为同分异构体
B.四种生育三烯酚均可使酸性高锰酸钾溶液褪色
C.四种生育三烯酚的结构中均不存在手性碳原子
D.1 mol α?生育三烯酚与溴的四氯化碳溶液发生反应,理论上最多可消耗3 mol Br2