题目内容
现有下列电解质溶液:① Na2CO3 ② NaHCO3 ③ 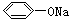 ④CH3COONH4 ⑤NH4HCO3
④CH3COONH4 ⑤NH4HCO3
已知酸性H2CO3 > > HCO3-
> HCO3-
(1)常温下,物质的量浓度相同的① 、②、③溶液pH大小顺序为(填写序号):_____>_____>_____。
(2)写出⑤与足量NaOH溶液混合加热反应的离子方程式____________________。
(3)已知常温下CH3COONH4溶液呈中性,根据这一事实推测⑤溶液的pH_____7(填>、=或<)
(4)在温度t ℃时,pH=3的某水溶液中c(OH-)=10-9 mol/L在此温度下pH均为4的盐酸和(NH4)2SO4溶液中由水电离出的c(H+)之比为_________。
(5)将标准状况下的4.48 L氨气完全溶解在含0.1 mol HCl的水溶液中形成1 L溶液,所得溶液pH=9,其中离子浓度由大到小的顺序是_______________。
(6)常温下,pH=10的强碱AOH和pH=4的酸HnB等体积混合后溶液显酸性, AOH与HnB完全中和所得溶液呈_________性,其原因用离子方程式表示为__________________________。
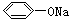 ④CH3COONH4 ⑤NH4HCO3
④CH3COONH4 ⑤NH4HCO3 已知酸性H2CO3 >
 > HCO3-
> HCO3- (1)常温下,物质的量浓度相同的① 、②、③溶液pH大小顺序为(填写序号):_____>_____>_____。
(2)写出⑤与足量NaOH溶液混合加热反应的离子方程式____________________。
(3)已知常温下CH3COONH4溶液呈中性,根据这一事实推测⑤溶液的pH_____7(填>、=或<)
(4)在温度t ℃时,pH=3的某水溶液中c(OH-)=10-9 mol/L在此温度下pH均为4的盐酸和(NH4)2SO4溶液中由水电离出的c(H+)之比为_________。
(5)将标准状况下的4.48 L氨气完全溶解在含0.1 mol HCl的水溶液中形成1 L溶液,所得溶液pH=9,其中离子浓度由大到小的顺序是_______________。
(6)常温下,pH=10的强碱AOH和pH=4的酸HnB等体积混合后溶液显酸性, AOH与HnB完全中和所得溶液呈_________性,其原因用离子方程式表示为__________________________。
(1)①>③>②
(2)NH4++HCO3-+2OH- NH3↑+CO32-+2H2O
NH3↑+CO32-+2H2O
(3)>
(4)1:104
(5)c(NH4+)>c(Cl-)>c(OH-)>c(H+)
(6)碱;Bn-+H2O HBn-1+OH-
HBn-1+OH-
(2)NH4++HCO3-+2OH-
 NH3↑+CO32-+2H2O
NH3↑+CO32-+2H2O (3)>
(4)1:104
(5)c(NH4+)>c(Cl-)>c(OH-)>c(H+)
(6)碱;Bn-+H2O
 HBn-1+OH-
HBn-1+OH- 
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
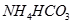 (已知酸性
(已知酸性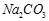 ②
②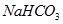 ?③
?③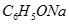 ? ④
? ④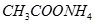 ⑤
⑤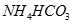 (已知酸性
(已知酸性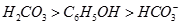 。)
。)