题目内容
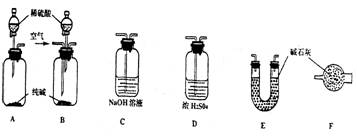
某工业纯碱中含有少量NaCl和NaOH.为测定其中Na2CO3的质量分数:甲、乙、丙、丁四位同学选择上述装置分成(1)、(2)两组,对实验进行设计、讨论:
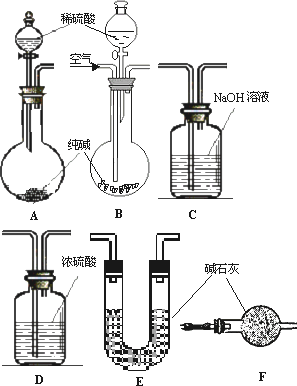
(1)甲将A、E连接,使Na2CO3与稀硫酸反应生成的CO2被E中的碱石灰吸收,测定反应前和反应后E的总质量差,求出Na2CO3的质量分数.
乙认为甲应在A、E之间再连接装置D,目的是________.
(2)丙将B、D、E连接,Na2CO3与稀硫酸完全反应后,从B的导管口缓缓鼓入空气,目的是________.
丁认为空气中含有CO2,丙直接向B中鼓入空气会使测定结果________(填“偏高”、“偏低”、“无影响”).因此,应将鼓入的空气先通过装置________,并且在E后还应连接装置F,防止空气中的水和CO2进入E装置.
四位同学通过讨论最终认为第(2)小组测定的数据更为准确,数据如下:
通过计算,该工业纯碱中Na2CO3的质量分数为________﹪(保留两位小数).
答案:

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目