��Ŀ����
��12�֣�MnSO4��H2O�ڹ�ҵ��ũҵ�ȷ����й㷺��Ӧ�á�
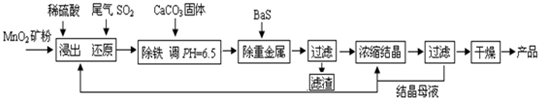
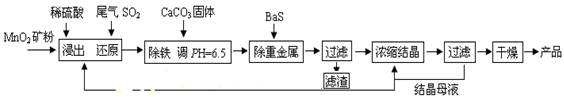
��һ���Ʊ�����ҵ���û�����β���е�Ũ��SO2��ԭMnO2���Ʊ�MnSO4��H2O�������£�
��֪�� ����ʱ�������������ε�Ksp��CuS--6.3��10-36��PbS--1.0��10-28��NiS--2.0��10-26��MnS--2.5��10-10����ش��������⣺
��1��������MnO2������Ŀ���� ����2���������������ӷ�Ӧ����ʽΪ ��
��3�����ؽ������Ӻ��������Һ��Cu2+��Pb2+��Ni2+��Ũ�Ⱦ�Ϊ1.0��10-5mol/L����c(S2-)���= mol/L��
�����������ʡ����ȶ��ԣ�MnSO4��H2O��1150������·ֽ�IJ�����Mn3O4�������ˮ���ڸ������������̾���ֽⷴӦ�Ļ�ѧ����ʽ��
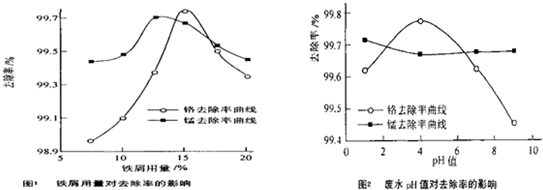
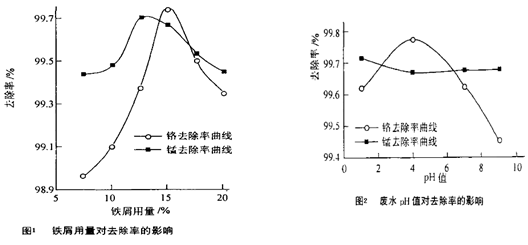
��������ˮ������������ˮ����Ҫ��ȾΪMn2+��Cr6+�����о���м������pHֵ�Է�ˮ�и�����ȥ���ʵ�Ӱ�죬��1��ȡ100mL��ˮ��250mL����ƿ�У�����pHֵ���涨ֵ���ֱ���벻ͬ���ķ���м���õ���м�����Ը�����ȥ���ʵ�Ӱ������ͼ1��ʾ������pHһ��ʱ����ˮ����м����Ϊ ʱ�̡���ȥ�������
��2��ȡ100mL��ˮ��250 mL����ƿ�У�����涨�������ۣ����ɲ�ͬ��pHֵ���õ�pHֵ�Ը�����ȥ���ʵ�Ӱ������ͼ2��ʾ��������м����һ��ʱ����ˮpH= ʱ�̡���ȥ�������
��ÿ��2�ֹ�12�֣�
��1������Ӧ��Ӵ�������ӿ췴Ӧ���ʣ�
��2��2Fe3+ + 3H2O+ 3CaCO3 = 2Fe(OH)3��+ 3CO2��+ 3Ca2+
���� Fe3+ + 3H2O = Fe(OH)3��+3H+ 2H+ + CaCO3 = Ca2++ CO2��+ H2O ��
��3��6.3��10-31
������3MnSO4��H2OMn3O4+ SO2��+ 2SO3��+ 3H2O
������15% 4
����:

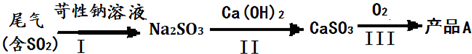

 Fe��OH��3+3H+ 2H++CaCO3=Ca2++CO2��+H2O
Fe��OH��3+3H+ 2H++CaCO3=Ca2++CO2��+H2O Mn3O4+SO2��+2SO3��+3H2O
Mn3O4+SO2��+2SO3��+3H2O