��Ŀ����
�Զ��Ե缫���NaCl��Һ��CuSO4��Һ���õ����ֲ���A��B��C��������֮���ת����ϵ����ͼ��ʾ��ͼ �в��뷴Ӧ�����ɵ�ˮ������ȥ������֪���Ƕ�����Ԫ�صĵ��ʣ������ճ������г��õİ�װ���ϡ�
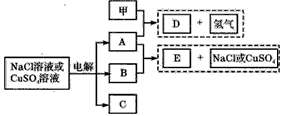
�ش��������⣺
(1)����Ԫ�����ڱ���λ����____��
(2)��������NaCl��Һ����A��B��Ӧ�����ӷ���ʽ��___��
�������100mL0. 1mol��L-1NaCl��Һ������������������112mL���壨��״��������������Һ��pHΪ ____�����Է�Ӧǰ����Һ������仯����
(3)��������CuSO4��Һ��
��E�Ļ�ѧʽ��____�����ʱ�����ĵ缫��Ӧʽ��____ ��
�ڼ���ʱ��A��Ũ��Һ����B������Ӧ��A��Ũ����ʱ��仯��ͼ����ȷ��___��
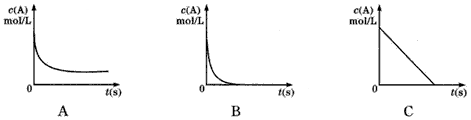
�������÷�ӦA+B+C��CuSO4+H2O�ѻ�ѧ��ת��Ϊ���ܣ�����Ƶ�صĸ���������____����Ԫ�ط��ţ���
(1)��3���ڵڢ�A��
(2)��Cl2 +2OH-==Cl-+ClO-+H2O ����13
(3)��SO2 ��4OH--4e-==O2��+2H2O����A����Cu

��ϰ��ϵ�д�
�����Ŀ
NA���������ӵ�����������˵���в���ȷ����
| A��100 mL 0.5 mol/L��������Һ�У�������ӵ���ĿС��0.05 NA |
| B����״���£�22.4 Lˮ�������еķ�����ΪNA |
| C��0.8 mol�����к�4.8 NA����ԭ�� |
| D���ö��Ե缫����Ȼ�ͭ��Һʱ������������64g������ʯī��Ϊ�����ܲ���NA���������� |