题目内容
2.用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一种物质(括号内),溶液不能与原来溶液完全一样的是( )| A. | CuSO4(CuO) | B. | KNO3(H2O) | C. | NaCl(HCl) | D. | KI(H2O) |
分析 A.电解硫酸铜溶液生成铜、氧气和硫酸,结合两极生成的物质选择加入的试剂;
B.电解KNO3溶液生成氢气和氧气;
C.电解氯化钠溶液生成氢氧化钠、氯气和氢气;
D.电解KI溶液生成氢氧化钾、碘单质和氢气.
解答 解:A.惰性电极电解硫酸铜溶液,生成物是铜、氧气和硫酸,所以需要加入的是氧化铜或碳酸铜,故A正确;
B.电解KNO3溶液生成氢气和氧气,要复原加入的应该是水,故B正确;
C.电解氯化钠溶液生成氢气、氯气和氢氧化钠溶液,需要加入的是HCl,故C正确;
D.电解KI溶液生成氢氧化钾、碘单质和氢气,需要加入的是HI,故D错误.
故选D.
点评 本题考查了电解原理应用,侧重考查学生分析问题、解决问题的能力,有助于培养学生的逻辑思维能力和发散思维能力.该题的关键是准确判断电极产物并能灵活运用,该题是中等难度的试题,也是高考中的常见考点,试题基础性强.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.一定温度下,在某密闭容器中发生反应:2HI(g)?H2(g)+I2(s)△H>0,若 0~15s 内 c(HI)由 0.1mol,•L-1 降到 0.07mol•L-1,则下列说法正确的是( )
| A. | 0~15 s 内用 I2 表示的平均反应速率为:v(I2)=0.001 mol•L-1•s-1 | |
| B. | c(HI)由 0.07 mol•L-1 降到 0.05 mol•L-1 所需的反应时间小于 10 s | |
| C. | 升高温度正反应速率加快,逆反应速率减慢 | |
| D. | 减小反应体系的体积,化学反应速率加快 |
10.下列有关表述正确的是( )
| A. | 位于短周期的X元素的阳离子与Y元素的阴离子具有相同的电子层结构,则两元素的最高正化合价一定是X<Y | |
| B. | 对于某元素的单质,若它的氧化性弱,那么它的还原性一定强 | |
| C. | 热稳定性:AsH3<PH3<H2O<HF | |
| D. | 最外层电子数较少的金属元素,一定比最外层电子数较多的金属元素活泼性强 |
17.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1 molCl2参加反应转移电子数一定为2NA | |
| B. | 7.8gNa2O2中含有的阴离子数为0.1NA | |
| C. | 标准状况下,5.6 L四氯化碳含有的分子数为0.25NA | |
| D. | 1 mol FeCl3跟水完反应转化为氢氧化铁胶体,其中胶体粒子的数目为NA |
7.下列说法正确的是( )
| A. | 天然橡胶 和杜仲胶 和杜仲胶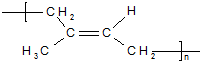 属于同分异构体 属于同分异构体 | |
| B. | 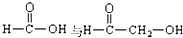 属于同系物 属于同系物 | |
| C. | 合成 的单体为乙烯和2-丁烯 的单体为乙烯和2-丁烯 | |
| D. | 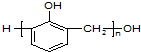 是由苯酚和甲醛发生加成反应后的产物脱水缩合而成 是由苯酚和甲醛发生加成反应后的产物脱水缩合而成 |
14.下列物质既含有离子键,又含有共价键的是( )
| A. | H2 | B. | NaOH | C. | MgCl2 | D. | HCl |
12.可用来检验酒精中是否含水的试剂是 ( )
| A. | 硫酸铜溶液 | B. | 无水硫酸铜 | C. | 金属钠 | D. | 新制生石灰 |
 (并用双线桥标出电子转移的方向和数目),其中氧化产物为Ca(ClO)2(写化学式).
(并用双线桥标出电子转移的方向和数目),其中氧化产物为Ca(ClO)2(写化学式).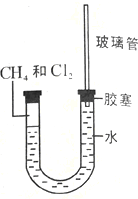 已知:卤素的氢化物易溶于水.某同学采用如图所示装置研究氯气与甲烷反应.实验时,往U型管的左端装入甲烷和氯气(体积比为1:4)的混合气体,并将该装置放置在光亮处,让混合气体缓慢地反应一段时间.根据要求回答问题:
已知:卤素的氢化物易溶于水.某同学采用如图所示装置研究氯气与甲烷反应.实验时,往U型管的左端装入甲烷和氯气(体积比为1:4)的混合气体,并将该装置放置在光亮处,让混合气体缓慢地反应一段时间.根据要求回答问题: A.氢原子数为十二 B.一氯取代物只有一种结构.
A.氢原子数为十二 B.一氯取代物只有一种结构.