题目内容
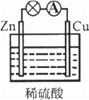
【题目】合成新型高分子M的路线如图: 
为了测定上述转化流程中有机物H的结构,做如下实验:
①将2.3g有机物H完全燃烧,生成0.1molCO2和2.7g水
②H的质谱图和核磁共振氢谱图分别为图1和图2: 
试回答下列问题:
(1)有机物H中官能团的名称 .
(2)A的分子式是C7H8 , 反应①的化学方程式: .
(3)E的分子式是C6H10O2 , E的结构简式为 .
(4)试剂b是 , 反应④的反应类型是 .
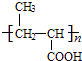
(5)反应⑥的化学方程式: .
(6)已知: 以H为起始原料,选用必要的无机试剂合成E,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件) .
【答案】
(1)羟基
(2)![]() +HO﹣NO2
+HO﹣NO2![]()
![]() +H2O
+H2O
(3)CH3CH=CHCOOCH2CH3
(4)NaOH水溶液、加热;加聚反应
(5)n ![]() +
+ 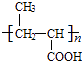
![]()
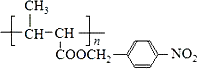 +nH2O
+nH2O
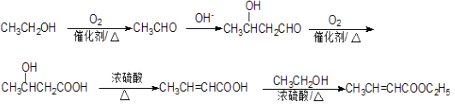
(6)
【解析】解:(1)由上述分析可知,有机物H为乙醇,官能团的名称羟基,所以答案是:羟基;(2)A的分子式是C7H8,反应①为甲苯的硝化反应,化学方程式为 ![]() +HO﹣NO2
+HO﹣NO2 ![]()
![]() +H2O,
+H2O,
所以答案是: ![]() +HO﹣NO2
+HO﹣NO2 ![]()
![]() +H2O;(3)E的分子式是C6H10O2,E的结构简式为CH3CH=CHCOOCH2CH3,所以答案是:CH3CH=CHCOOCH2CH3;(4)C在氢氧化钠水溶液、加热条件下发生水解反应生成D为
+H2O;(3)E的分子式是C6H10O2,E的结构简式为CH3CH=CHCOOCH2CH3,所以答案是:CH3CH=CHCOOCH2CH3;(4)C在氢氧化钠水溶液、加热条件下发生水解反应生成D为 ![]() ,试剂b是NaOH水溶液、加热,反应④为E→F,反应类型是加聚反应,
,试剂b是NaOH水溶液、加热,反应④为E→F,反应类型是加聚反应,
所以答案是:NaOH水溶液、加热;加聚反应;(5)反应⑥的化学方程式为n ![]() +
+ 
![]()
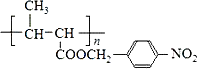 +nH2O,
+nH2O,
所以答案是:n ![]() +
+ 
![]()
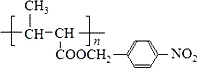 +nH2O;(6)E为CH3CH=CHCOOCH2CH3,则需要合成CH3CH=CHCOOH和CH3CH2OH,CH3CH2OH氧化生成CH3CHO,CH3CHO发生信息反应
+nH2O;(6)E为CH3CH=CHCOOCH2CH3,则需要合成CH3CH=CHCOOH和CH3CH2OH,CH3CH2OH氧化生成CH3CHO,CH3CHO发生信息反应 ![]() 再消去即可生成CH3CH=CHCOOH,所以合成流程图为
再消去即可生成CH3CH=CHCOOH,所以合成流程图为 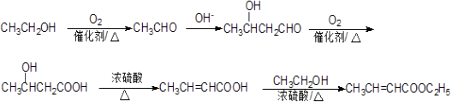 (第三、四步顺序可调换),
(第三、四步顺序可调换),
所以答案是:  .
.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案【题目】沉淀转化广泛应用于工业生产和科学实验。为了探究AgCl、Ag2S(黑色)的溶解性及转化等相关性质,做以下实验:
步 骤 | 现 象 |
Ⅰ.将NaCl溶液滴入AgNO3溶液中至恰好完全反应。 | 产生白色沉淀。 |
Ⅱ.过滤出Ⅰ中的白色沉淀置于试管中,在试管中加入过量Na2S溶液并充分振荡。 | 白色沉淀变为黑色。 |
Ⅲ.过滤出Ⅱ中的黑色沉淀置于试管中,在试管中加入过量的NaCl溶液并充分振荡后静置。 | 沉淀由黑色最后完全变为乳白色。 |
回答下列问题:
(1)Ⅰ中的白色沉淀是__________。
(2)写出Ⅱ中沉淀变黑的离子方程式__________ ,沉淀转化的主要原因是______________。
(3)滤出步骤Ⅲ中的乳白色沉淀,加入过量的浓HNO3使之充分反应,有红棕色气体生成,尚有部分沉淀未溶解,过滤得到滤液X和白色沉淀Y。
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀;
ⅱ.将Y与足量的KI溶液充分混合,白色沉淀最终转化为黄色沉淀。
① 由ⅰ判断,滤液X中被检出的离子是_______。
② 由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有__________和__________。
(4)为了证明实验步骤Ⅲ中的黑色沉淀只有在NaCl存在下,才能和氧气反应转化为乳白色沉淀,设计了如下对照实验并将实验结果记录在右侧的表格中。
装置 | 实验结果 |
B | 一段时间后,出现乳白色沉淀 |
C | 一段时间后,无明显变化 |
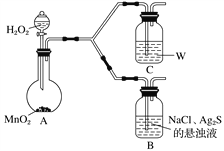
①A中,盛有MnO2的玻璃仪器名称是_________________。
②C中盛放的是物质W的悬浊液,W是________(填化学式)。
③请完成B中发生反应的反应式并配平:_____
Ag2S+ + + H2O![]() AgCl+ + NaOH
AgCl+ + NaOH
________
【题目】氢气是21世纪的新型能源.制氢的方法之一是以煤的转化为基础,部分反应如下: CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣41kJmol﹣1
CaO(s)+CO2(g)CaCO3(s)△H=﹣172kJmol﹣1
CO2(g)+4H2(g)CH4(g)+2H2O(g)△H=﹣187kJmol﹣1
(1)写出CO与H2生成CH4和水蒸气的热化学方程式 .
(2)某温度下,在10L密闭容器中投入CO2、H2和CaO,仅发生CO2(g)+4H2(g)CH4(g)+2H2O(g)和CaO(s)+CO2(g)CaCO3(s)两个反应,部分物质的物质的量与时间的关系如表所示:
物质 | CO2 | H2 | CaO |
0 | 0.50 | 1.00 | 0.40 |
2 | 0.35 | 0.60 | a |
6 | 0.20 | 0.20 | b |
8 | 0.20 | 0.20 | b |
①反应在0~2min内的平均反应速率v(H2)=
②b=
③反应到达平衡后,改变反应的某些条件,再次达到平衡时,不正确的是(填字母)
A.扩大容器体积c(H2)增大 B.升高温度,n(CO2)增大
C.充入少量H2 , CaCO3质量减小 D.充入少量CO2 , c(CH4)增大
④此温度下,反应CO2(g)+4H2(g)CH4(g)+2H2O(g)的化学平衡常数K= . 若向10L容器中投入CO2、H2和CH4各0.1mol,H2O(g)xmol,要使v正(CO2)>v逆(CO2),x的取值范围为
(3)若以CH4、O2组成燃料电池,在酸性条件下负极电极反应式为.当两极消耗3.36L气体(标准状况)时,将产生的气体(假设全部逸出)通入50mL2molL﹣1 NaOH溶液中,下列说法正确的是
A.反应过程中共转移电子1.2mol
B.所得溶液为Na2CO3和NaHCO3的混合溶液
C.c(Na+ )>c(CO32﹣)>c(OH﹣ )>c(HCO3﹣)>c(H+)
D.c(OH﹣)=2c(H2CO3)+c(HCO3﹣ )+c(H+ )