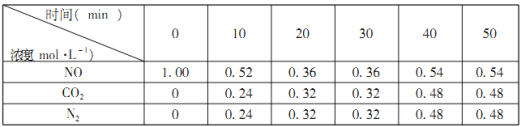
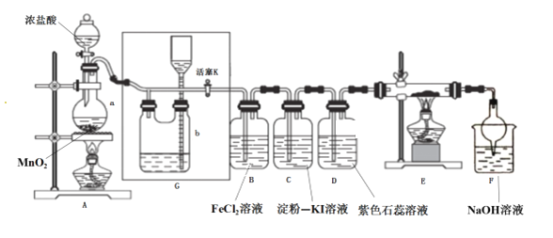
��Ŀ����
����Ŀ���������һ����Ҫ�ķǽ������ϣ��Ʊ��������Ҫ�������£�
�ٸ�������̼��ԭ���������Ƶôֹ衣
�ڴֹ������ HCl���巴Ӧ�Ƶ� SiHCl3��Si + 3HCl![]() SiHCl3+ H2
SiHCl3+ H2
��SiHCl3����� H2�� 1000 ~1100�淴Ӧ�Ƶô���
��֪ ��SiHCl3���� H2Oǿ�ҷ�Ӧ���ڿ���������ȼ����ͨ������6000C�����ڻ���
��ش��������⣺
��1���ڢٲ��Ʊ��ֹ�Ļ�ѧ��Ӧ����ʽΪ __________________��
��2���ֹ���HCl��Ӧ��ȫ�����������õ���SiHCl3���е� 33.0�棩�к������� SiCl4���е�57.6�棩
�� HCl���е�-84.7�棩���ᴿ SiHCl3���õķ���Ϊ_________________________��
��3���� SiHCl3����� H2��Ӧ�Ʊ������װ�����£���Դ���г�װ����ȥ����
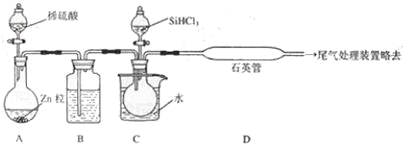
��װ�� B�е��Լ��� ___________�� װ�� C�е���ƿ��Ҫ���ȣ���Ŀ����__________________��
�ڷ�Ӧһ��ʱ���װ�� D�й۲쵽�������� _________________��װ�� D���ܲ�����ͨ�����ܵ�ԭ����__________________ ��װ��D�з�����Ӧ�Ļ�ѧ����ʽΪ_______________��
��Ϊ��֤�Ʊ�����ʵ��ijɹ��������Ĺؼ��Ǽ��ʵ��װ�õ������ԣ����ƺ÷�Ӧ�¶��Լ�____________________��
��Ϊ������Ʒ�����Ƿ��������ʣ���������ϡ�����ܽ⣬ȡ�ϲ���Һ�����ټ�����Լ�����д��ĸ���ţ���____________��
A ��ˮ B ��ˮ C NaOH��Һ D KSCN��Һ E Na2SO3 ��Һ
���𰸡�SiO2+2C![]() Si+2CO�� �������� Ũ���� ʹ������ƿ�е� SiHCl3���� �й����������� �ڷ�Ӧ�¶��£���ͨ���������� SiHCl3+H2
Si+2CO�� �������� Ũ���� ʹ������ƿ�е� SiHCl3���� �й����������� �ڷ�Ӧ�¶��£���ͨ���������� SiHCl3+H2![]() Si+3HCl �ž�װ���еĿ��� BD
Si+3HCl �ž�װ���еĿ��� BD
��������
��1�������£�̼�Ͷ������跴Ӧ���ɹ��һ����̼��
��2�������������ݣ����÷����ᴿSiHCl3��
��3�������ɵ���������ˮ��������ŨH2SO4������ȴ�ʹSiHCl3��������SiHCl3��������Ӧ�й赥�����ɣ����ݹ����ɫ�ж�Dװ���е���ɫ�仯����Ӧ�¶Ƚϸߣ���ͨ������������SiHCl3��H2��Ӧ���ɹ���Ȼ��⣻�������ǿ�ȼ�����壬�ײ�����ը��Ϊ��ֹ��ȫ�¹ʵķ�����������ͨһ��ʱ��H2����װ���еĿ����ž�����ȡ������Ʒ���Թ��м������ܽ⣬�ٵμ���ˮ��KSCN��aq���������ֺ�ɫ˵����Fe���������ֺ�ɫ˵������Fe��
��1�������£�̼�Ͷ������跴Ӧ���ɹ��һ����̼����Ӧ����ʽΪSiO2+2C![]() Si+2CO����
Si+2CO����
��2��SiHCl3���е�33.0�棩�к�������SiCl4���е�57.6�棩��HCl���е�-84.7�棩�����ڷе���ϴ���ͨ�������ȥ���ʡ�
��3����п��ϡ����ķ�Ӧ�Ƿ��ȷ�Ӧ���������ɵ���������ˮ������Ϊ����������һ��ѡ��ŨH2SO4�������ķ�Ӧ���ʽϴ����Լ��ȵ�Ŀ����ʹ������ƿ�е� SiHCl3������
�ڸ����£�SiHCl3��������Ӧ���ɹ赥�ʣ��赥���ǻҺ�ɫ���壬����Dװ���е��������й����������ɣ����ڸ����£���ͨ����������������ʹ��ʯӢ��������Ӧ����ʽΪSiHCl3+H2= Si+3HCl��
�������ǿ�ȼ�����壬�����������ﵽһ��ʱ�ײ�����ը��Ϊ��ֹ��ȫ�¹ʵķ�����������ͨһ��ʱ��H2���ž�װ���еĿ�����
�����ܺ��ᷴӦ�����������ӣ����������л�ԭ�ԣ����������ܱ���ˮ�������������ӣ������������軯����Һ���ɫ�����Կ�������ˮ�����軯����Һ�������Ĵ��ڣ���ѡBD��

 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д�