题目内容
在273℃、202kPa时,将44.8升NH3与128克O2混合后,充入一密闭容器,加Pt并升温至700℃,充分反应后,冷却到室温。
(1)在室温下得到的产物是什么?
(2)若该产物密度为1.44克/毫升,则其百分比浓度和物质的量浓度各为多少?(保留3位有效数字)
(1)HNO3和水
(2)77.8%,17.8 mol/L
解析:
涉及的化学方程式有:NH3+O2→NO+H2O(未配平)NO+O2→NO2,NO2+H2O→HNO3+NO,公式:PV=nRT。
![]()
设NH3全部转化为HNO3,总方程式有:
NH3+2O2==HNO3+H2O
1 2 1 1
![]()
题中所给数据,表明NH3与O2理论上恰好完全反应,生成HNO3和H2O,且为1∶1关系,原假设成立。
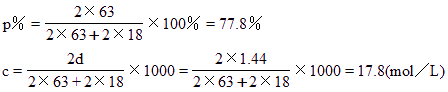
由此题解析过程表明,对于有多步反应的计算,从整体角度考虑,判断是否过量,更简捷。</PGN0106A.TXT/PGN>

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目