题目内容
铁氧体是一类磁性材料,通式为MO· xFe2O3(M为二价金属离子)。
根据题意完成:
(1)为了制备铁氧体,称取5.6g铁粉、一定量的FeCl3(s) 作为原料,先制备Fe3O4。方法如下:用稀硫酸溶解铁粉,加入FeCl3(s),经过一系列反应得到纯净的Fe3O4 [ 已知1molFe(OH)2与2molFe(OH)3混合灼烧可得到1mol Fe3O4 ]。需要加入FeCl3(s) g。
(2)如果以MgSO4(s)和FeCl3(s)为原料制备9.0 g MgO· 2Fe2O3,在制取过程中至少需要1 mol/L的NaOH(aq)
mL。
(3)在一次制备Fe3O4的实验中,由于反应物比例控制不当,获得了另一种产品。取a克该产品溶于100mL盐酸(足量)中,需要通入672 mL(标准状况)Cl2才能把溶液中的Fe2+ 全部氧化为Fe3+,然后蒸干所得溶液,灼烧至恒重,得9.6 g固体。计算:
①ag 该产品溶于盐酸后,溶液中Fe2+ 的物质的量浓度(溶液体积变化忽略不计)。
②推算该产品的化学式(写出推算过程)。
(4)有一种在电子工业广泛应用的含铬铁氧体,其组成可表示为:Fe2+ · Fe3+[ Fe3+(1-x) · Cr3+x · O4]。向含有1.92 mol硝酸的某溶液中加入一定量的该种铁氧体,恰好完全反应后,收集到NO、NO2的混合气体2.688 L(标准状况)。计算:(均需写出计算过程)
①参加反应的铁氧体的物质的量。
②所得气体中NO、NO2的体积比。
(1)32.5 g(3分)
(2)350mL(2分,1分)
(3)①0.6 mol/L(1分×2) ②2FeO · Fe2O3(1分×3)
(4)①0.2 mol(1分×2) ②V(NO):V(NO2)=1:2(1分×3)
【解析】
试题分析:(1)按题中所给,1molFe(OH)2与2molFe(OH)3混合灼烧可得到1mol Fe3O4其中,Fe(OH)2来自铁粉,Fe(OH)3来自FeCl3。为达到1:2的关系,需要氯化铁0.2mol,质量 32.5g。
(2) 9.0g的MgO 2Fe2O3 共0.025mol,其中有0.025molMg2+ 、0.1molFe3+,需要NaOH 0.35mol ,即题中溶液350ml;
(3)①氯气的物质的量为 =0.03mol,氯气氧化Fe2+为Fe3+,根据电子转移守恒可知Fe2+的物质的量为
=0.03mol,氯气氧化Fe2+为Fe3+,根据电子转移守恒可知Fe2+的物质的量为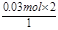 =0.06mol,故氧化物中+2价铁的物质的量为0.06mol,溶液中Fe2+ 的物质的量浓度0.6 mol/L;②最后所得为氯化铁溶液,蒸干溶液,灼烧至恒重,得9.6g固体为Fe2O3,Fe2O3的物质的量为
=0.06mol,故氧化物中+2价铁的物质的量为0.06mol,溶液中Fe2+ 的物质的量浓度0.6 mol/L;②最后所得为氯化铁溶液,蒸干溶液,灼烧至恒重,得9.6g固体为Fe2O3,Fe2O3的物质的量为 =0.06mol,利用铁元素守恒可知氧化物中+3价铁的物质的量为0.06mol×2-0.06mol=0.06mol,故FeO与Fe2O3的物质的量之比为0.06mol:
=0.06mol,利用铁元素守恒可知氧化物中+3价铁的物质的量为0.06mol×2-0.06mol=0.06mol,故FeO与Fe2O3的物质的量之比为0.06mol: =2:1,该产品化学式为2FeO•Fe2O3,故答案为:2FeO•Fe2O3;(4)①根据题目的分子式,那其中的X只能取1,其他情况皆不符合,一个分子中不可能有半个铬离子,然后就可以得到分子式了,为Fe2+Fe3+[ Cr3+· O4]。,可以看出,分子式中的铁元素数目为铬元素数目的2倍。然后,根据溶液电荷守恒定律,有3n(Fe3+)+3n(Cr3+)=n(NO3-),根据氮元素守恒,拿硝酸的量减去溢出气体的量2.688/22.4即为溶液中氮元素的量,也即1.92-0.12=1.8mol,为溶液中硝酸跟的浓度,那么根据电荷守恒式和n(Fe3+)=2(Cr3+),可以得到n(Cr3+)=0.2mol。一个铬铁氧体分子中分子中只有一个铬原子,他俩是一比一关系,那么消耗铬铁氧体的量就是0.2mol。
=2:1,该产品化学式为2FeO•Fe2O3,故答案为:2FeO•Fe2O3;(4)①根据题目的分子式,那其中的X只能取1,其他情况皆不符合,一个分子中不可能有半个铬离子,然后就可以得到分子式了,为Fe2+Fe3+[ Cr3+· O4]。,可以看出,分子式中的铁元素数目为铬元素数目的2倍。然后,根据溶液电荷守恒定律,有3n(Fe3+)+3n(Cr3+)=n(NO3-),根据氮元素守恒,拿硝酸的量减去溢出气体的量2.688/22.4即为溶液中氮元素的量,也即1.92-0.12=1.8mol,为溶液中硝酸跟的浓度,那么根据电荷守恒式和n(Fe3+)=2(Cr3+),可以得到n(Cr3+)=0.2mol。一个铬铁氧体分子中分子中只有一个铬原子,他俩是一比一关系,那么消耗铬铁氧体的量就是0.2mol。
②这题的可以利用氧化还原知识来解,因为生成NO、NO2的反应为二价铁离子和硝酸的反应,分别写出两个反应的离子反应方程式,然后设生成NO为Xmol,NO2为ymol,根据生成气体总量,可知x+y=2.688/22.4=0.12,然后根据反应式的对应关系,根据二价铁(等于消耗铬铁氧体的量)的含量为3x+y=0.2,联立方程解出得x = 0.04 y = 0.08,则x:y-1:2,V(NO):V(NO2)=1:2。
考点:本题以铁氧体磁性材料制备为载体,考查混合物的有关计算,难度中等,注意根据元素守恒与极限法进行解答。

 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案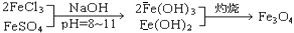
 ,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为 。
,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为 。
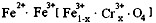 ,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为 。
,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为 。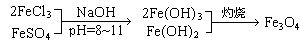
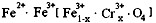 ,现有15.2
g
FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为
。
,现有15.2
g
FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为
。