题目内容
4.复盐NH4Fe(SO4)2俗称铁铵矾,下列有关其溶液的叙述正确的是( )| A. | 该溶液中K+、Mg2+、H+、NO3-不能大量共存 | |
| B. | 溶液中的NH4+与Fe3+均发生水解反应,且相互促进 | |
| C. | 加入金属铜与Fe3+反应的离子方程式为:2Fe3++3Cu=2Fe+3Cu2+ | |
| D. | 向其中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:NH4++Fe3++2SO42-+2Ba2++4OH-=2BaSO4↓+NH3•H2O+Fe(OH)3↓ |
分析 A.NH4Fe(SO4)2在溶液中电离出铵根离子、铁离子和硫酸根离子,四种离子之间不反应,都不与铵根离子、铁离子和硫酸根离子反应;
B.铵根离子和铁离子水解都生成氢离子,相互抑制水解;
C.铜与铁离子反应生成亚铁离子和铜离子,不会生成铁单质
D.硫酸根离子恰好沉淀时,硫酸铁铵与氢氧化钡的物质的量之比为1:2,据此写出反应的离子方程式.
解答 解:A.K+、Mg2+、H+、NO3-之间不反应,且都不与NH4Fe(SO4)2反应,在溶液中能大量共存,故A错误;
B.溶液中的NH4+与Fe3+均发生水解反应使溶液显示酸性,二者的水解是相互抑制的,故B错误;
C.加入金属铜与Fe3+反应生成亚铁离子和铜离子,正确的离子方程式为:2Fe3++Cu=2Fe2++Cu2+,故C错误;
D.向NH4Fe(SO4)2滴入Ba(OH)2溶液恰好使SO42-完全沉淀,铵根离子和铁离子也恰好反应,反应的离子方程式为:NH4++Fe3++2SO42-+2Ba2++4OH-=2BaSO4↓+NH3•H2O+Fe(OH)3↓,故D正确;
故选D.
点评 本题考查了离子共存的判断、离子方程式的书写及盐的水解原理及其影响等知识,题目难度中等,试题知识点较多,充分考查了学生的分析能力及灵活应用基础知识的能力,注意熟练掌握离子方程式的书写原则,明确判断离子方程式正误的常用方法.

练习册系列答案
相关题目
14.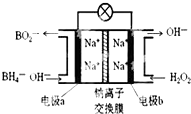 某新型电池NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示.下列说法正确的是( )
某新型电池NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示.下列说法正确的是( )
 某新型电池NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示.下列说法正确的是( )
某新型电池NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示.下列说法正确的是( )| A. | 电池工作时Na+从b极区移向a极区 | |
| B. | a极上的电极反应式为:BH4-+8OH--8e-=BO2-+6H2O | |
| C. | b极上的电极反应式为:H2O2+2e-+2H+=2H2O | |
| D. | 每消耗3molH2O2,转移3mole- |
 电量为(已知NA=6.02×1023mol-1,电子电荷为1.60×10-19C,列式表示即可)。
电量为(已知NA=6.02×1023mol-1,电子电荷为1.60×10-19C,列式表示即可)。


 ;D→E的反应类型取代反应.
;D→E的反应类型取代反应. .
. .
. )的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3.
)的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3.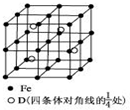 A、B、C、D分别代表四种不同的短周期元素.A、B元素原子的价电子排布分别为ns1、ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的p能级中有1个电子.
A、B、C、D分别代表四种不同的短周期元素.A、B元素原子的价电子排布分别为ns1、ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的p能级中有1个电子.