题目内容
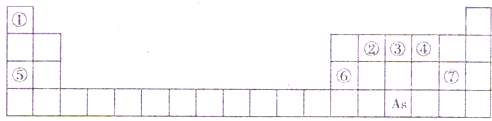
(2011?万州区一模)元素周期表是人们研究物质性质的重要工具.下表是元素周期表的一部分,A、B、C、D、E、X、Y是该表中给出元素组成的常见单质或化合物.
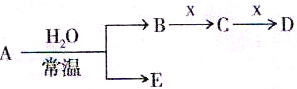
已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去):
(1)As在周期表中的位置
(2)若E为单质气体,D为白色沉淀,A的化学式可能是
(3)若E为氧化物,X是碱性盐溶液,C为无色无味的气体,且C分子中有22个电子,则A的化学式为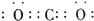
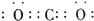 ,A与水反应的化学方程式为
,A与水反应的化学方程式为
(4)Y由④⑤⑦三种元素组成,它的水溶液是一种生活中常见的消毒剂.As可与Y的水溶液反应,生成As最高价含氧酸,该反应的化学方程式为

已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去):

(1)As在周期表中的位置
第四周期第VA族
第四周期第VA族
;(2)若E为单质气体,D为白色沉淀,A的化学式可能是
Na、Na2O2或NaH
Na、Na2O2或NaH
,B含有的化学键类型为离子键和极性共价键
离子键和极性共价键
,B与X反应的离子方程式为Al3++4OH-═AlO2-+2H2O
Al3++4OH-═AlO2-+2H2O
;(3)若E为氧化物,X是碱性盐溶液,C为无色无味的气体,且C分子中有22个电子,则A的化学式为
NO2
NO2
,C的电子式为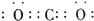
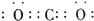
3NO2+H2O═2HNO3+NO
3NO2+H2O═2HNO3+NO
;(4)Y由④⑤⑦三种元素组成,它的水溶液是一种生活中常见的消毒剂.As可与Y的水溶液反应,生成As最高价含氧酸,该反应的化学方程式为
5NaClO+2As+3H2O═2H3AsO4+5NaCl
5NaClO+2As+3H2O═2H3AsO4+5NaCl
.分析:(1)As的原子序数为33,由原子结构来分析位置;
(2)根据表中的元素可知,只有⑤形成的物质与水反应生成氢气,碱与⑥的金属离子反应生成沉淀;
(3)根据表中的元素可知,只有③形成的物质与水反应生成NO气体符合,硝酸与碳酸盐生成二氧化碳分子,以此来分析;
(4)④为O,⑤为Na,⑦为Cl,则Y为NaClO,由As可与Y的水溶液反应,生成As最高价含氧酸来分析化学反应.
(2)根据表中的元素可知,只有⑤形成的物质与水反应生成氢气,碱与⑥的金属离子反应生成沉淀;
(3)根据表中的元素可知,只有③形成的物质与水反应生成NO气体符合,硝酸与碳酸盐生成二氧化碳分子,以此来分析;
(4)④为O,⑤为Na,⑦为Cl,则Y为NaClO,由As可与Y的水溶液反应,生成As最高价含氧酸来分析化学反应.
解答:解:(1)As的原子序数为33,原子结构中有四个电子层,最外层电子数为5,则As位于元素周期表中第四周期第VA族,故答案为:第四周期第VA族;
(2)根据表中的元素可知,只有⑤形成的物质与水反应生成氢气,则A可能为Na、Na2O2或NaH;与水反应生成的B为NaOH,钠离子与氢氧根离子以离子键结合,氢氧之间以共价键结合,即NaOH中存在离子键和极性共价键;白色沉淀为Al(OH)3,则B与X的反应为NaOH与氯化铝反应生成偏铝酸钠和水,离子反应为Al3++4OH-═AlO2-+2H2O,
故答案为:Na、Na2O2或NaH;离子键和极性共价键;Al3++4OH-═AlO2-+2H2O;
(3)根据表中的元素可知,只有③形成的物质与水反应生成NO气体符合,则A为NO2,A与水反应生成硝酸和一氧化氮,其反应为3NO2+H2O═2HNO3+NO,硝酸与碳酸盐反应生成二氧化碳,分子中有6+8×2=22个电子,符合题意,二氧化碳的电子式为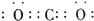 ,故答案为:NO2;
,故答案为:NO2;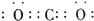 ;3NO2+H2O═2HNO3+NO;
;3NO2+H2O═2HNO3+NO;
(4)④为O,⑤为Na,⑦为Cl,则Y为NaClO,As最高价含氧酸为H3AsO4,由质量守恒定律及氧化还原反应可知还生成
NaCl,则化学反应为5NaClO+2As+3H2O═2H3AsO4+5NaCl,
故答案为:5NaClO+2As+3H2O═2H3AsO4+5NaCl.
(2)根据表中的元素可知,只有⑤形成的物质与水反应生成氢气,则A可能为Na、Na2O2或NaH;与水反应生成的B为NaOH,钠离子与氢氧根离子以离子键结合,氢氧之间以共价键结合,即NaOH中存在离子键和极性共价键;白色沉淀为Al(OH)3,则B与X的反应为NaOH与氯化铝反应生成偏铝酸钠和水,离子反应为Al3++4OH-═AlO2-+2H2O,
故答案为:Na、Na2O2或NaH;离子键和极性共价键;Al3++4OH-═AlO2-+2H2O;
(3)根据表中的元素可知,只有③形成的物质与水反应生成NO气体符合,则A为NO2,A与水反应生成硝酸和一氧化氮,其反应为3NO2+H2O═2HNO3+NO,硝酸与碳酸盐反应生成二氧化碳,分子中有6+8×2=22个电子,符合题意,二氧化碳的电子式为
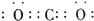 ,故答案为:NO2;
,故答案为:NO2;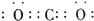 ;3NO2+H2O═2HNO3+NO;
;3NO2+H2O═2HNO3+NO;(4)④为O,⑤为Na,⑦为Cl,则Y为NaClO,As最高价含氧酸为H3AsO4,由质量守恒定律及氧化还原反应可知还生成
NaCl,则化学反应为5NaClO+2As+3H2O═2H3AsO4+5NaCl,
故答案为:5NaClO+2As+3H2O═2H3AsO4+5NaCl.
点评:本题考查元素周期表和元素周期律、无机物的推断,熟悉物质的性质、氧化还原反应等时解答本题的关键,难度较大.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
 (2011?万州区一模)图是钢铁在酸雨环境中腐蚀的示意图.有关说法正确的是( )
(2011?万州区一模)图是钢铁在酸雨环境中腐蚀的示意图.有关说法正确的是( )