题目内容
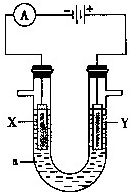
对如图所示的实验装置的判断中错误的是
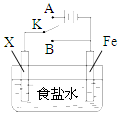
碳棒上发生的反应为2H++2e-=H2↑

| A.若X为碳棒,开关K置于A处可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀 |
| C.若X为锌棒,开关K置于B处时,为牺牲阳极的阴极保护法 |
| D.若X为碳棒,开关K置于B处时, |
D
试题分析:若开关K置于A处时,装置形成电解池,其中X为阳极,Fe为阴极,阴极被保护,可减缓铁的腐蚀,所以A正确,方程式为NaCl + H2O 电解 H2↑+ Cl2↑+ NaOH,若将开关置于B处时,装置形成原电池,当X为锌棒时,X为正极,Fe为负极,正极被保护,为牺牲阳极的阴极保护法,可减缓铁的腐蚀,所以B、C正确;当X\为碳棒时,X为正极,Fe为负极,负极:Fe - 2e- = Fe2+,正极:O2 + 2H2O + 4e- = 4OH-故选D。

练习册系列答案
相关题目