题目内容
【题目】将24.4gNaOH固体溶于水配成100 mL溶液,其密度为1.219g/mL。
(1)该溶液中NaOH的物质的量浓度为____。
(2)该溶液中 NaOH的质量分数为___。
(3)从该溶液中取出10mL,其中NaOH的物质的量浓度为____,NaOH的质量分数为____,含NaOH的质量为___,含NaOH的物质的量为___。
(4)将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为___。
【答案】6.1mol·L-1 20% 6.1mol·L-1 20% 2.44g 0.061mol 0.61mol·L-1
【解析】
(1)(1)根据n=m/M,c=n/V计算;
(2)根据m(溶液)=ρV,质量分数= ×100%计算;
×100%计算;
(3)溶液中浓度、质量分数与体积大小无关;根据n=cV,m=nM计算。
(4)根据稀释前后溶质的质量不变,列等式计算。
(1)24.4gNaOH的物质的量为:![]() =0.61mol,c(NaOH)=
=0.61mol,c(NaOH)=![]() =6.1mol·L-1。
=6.1mol·L-1。
答案:6.1mol·L-1
(2)100mLNaOH溶液的质量为:100mL×1.219g/mL=121.9g,NaOH的质量分数为:![]() ×100%≈20%。
×100%≈20%。
答案:20%
(3)由于溶液是均匀的,所以这10mL溶液与原100mL溶液相比,NaOH 的质量分数和溶液的密度及物质的量浓度均相同,即10mLNaOH溶液物质的量浓度为6.1mol/L,质量分数为20%;但NaOH的质量和物质的量均为原来的![]() ,含NaOH的质量为2.44g,物质的量为0.061mol。
,含NaOH的质量为2.44g,物质的量为0.061mol。
答案:6.1mol·L-1 20% 2.44g 0.061mol
(4)根据c1V1=c2V2,可知6.1mol/L×0.01L=c2×0.1L,可得c2=0.61mol/L;
答案:0.61mol·L-1

 金牌教辅培优优选卷期末冲刺100分系列答案
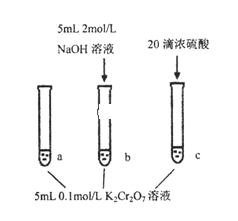
金牌教辅培优优选卷期末冲刺100分系列答案【题目】某同学研究浓度对化学平衡的影响,下列说法正确的是
已知:Cr2O72-(aq)(橙色)+H2O(l) | |
步骤: | 现象: 待试管b中颜色不变后与试管a比较, 溶液颜色变浅。 滴加浓硫酸,试管c温度略有升高, 溶液颜色与试管a相比,变深。 |
A. 该反应是一个氧化还原反应
B. 待试管b中溶液颜色不变的目的是使Cr2O72-完全反应
C. 该实验不能证明减小生成物浓度,平衡正向移动
D. 试管c中的现象说明影响平衡的主要因素是温度