题目内容
【题目】有可逆反应A+B![]() 2C在不同温度下经过一定时间,混合物中C的百分含量与温度关系如下图所示,那么:
2C在不同温度下经过一定时间,混合物中C的百分含量与温度关系如下图所示,那么:
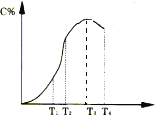
(1)反应在___________________温度下达到化学平衡;
(2)此反应在正反应为______________________热反应;
(3)由T1向T2变化时,V正____________V逆(填>、<、=);
(4)由T3向T4变化时,V正_____________V逆(填>、<、=)。
【答案】 T3 放 > <
【解析】(1)根据图像可知随着温度的升高,生成物C的含量逐渐增大,这说明此时反应并没有达到平衡状态,所以正反应速率大于逆反应速率。当C的含量达到最高时,T3时反应即达到化学平衡状态;(2)平衡后温度继续升高,C的含量反而降低,所以温度升高平衡向逆反应方向移动,说明逆反应速率大于正反应速率,正反应是放热反应;(3)从0到T3时刻前反应并没有达到平衡状态,所以正反应速率大于逆反应速率,即由T1向T2变化时,V正>V逆;(4)T3时反应即达到化学平衡状态,平衡后温度继续升高,平衡向逆反应方向移动,说明逆反应速率大于正反应速率,即由T3向T4变化时,V正<V逆。

练习册系列答案
相关题目