题目内容
医学上最近合成一种具有抗癌活性的化合物,该物质结构简式为
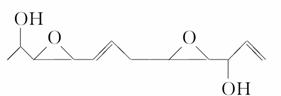
下列关于该化合物的说法正确的是
( )
A.分子式为C12H19O4
B.是乙醇的同系物
C.可发生氧化反应
D.处于同一平面的原子最多有5个
解析 分子式为C12H18O4,A错;乙醇的同系物应该是饱和一元醇,B错;该化合物分子中有碳碳双键和醇羟基,易被氧化,C正确;乙烯分子中的6个原子都在同一平面内,因此在含有碳碳双键的有机物分子中处于同一平面的原子至少有6个,D错。
答案 C

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
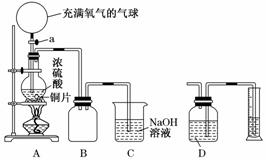
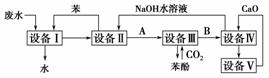
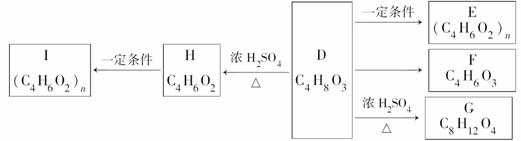 (1)D→H的反应类型: ______________________________;
(1)D→H的反应类型: ______________________________; ____。
____。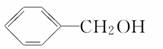
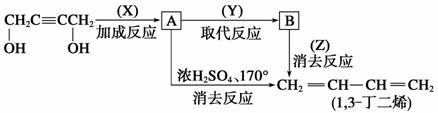
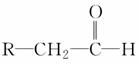 +
+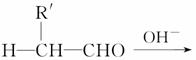
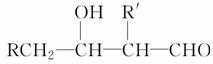
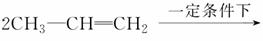
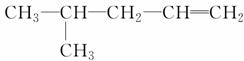
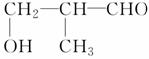 可由________和________两种有机物合成。
可由________和________两种有机物合成。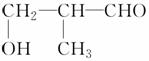 转变为
转变为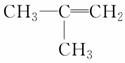 需经过________、________、________等较合理的反应类型。
需经过________、________、________等较合理的反应类型。 H++HClO+Cl-
H++HClO+Cl-