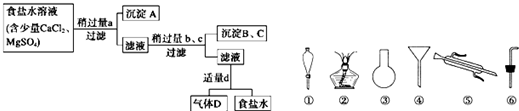
题目内容
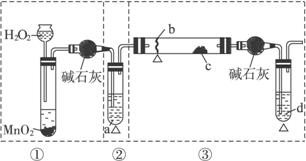
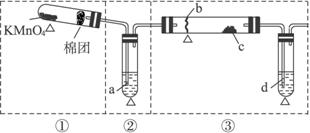
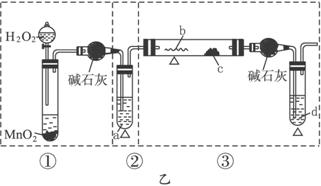
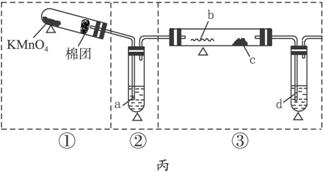
由如图仪器组成的一套制取SO2并验证它有氧化性、还原性和漂白性.(图中铁架台、铁夹等省略,装置③中E管气体向上流出)②④⑤装置中所用试剂只能从以下物质中选用:氯水、浓H2SO4、溴水、硝酸、品红溶液、烧碱溶液、石灰水.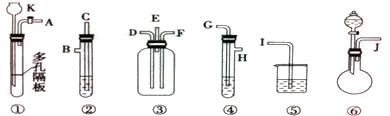
试回答:
(1)连接仪器时,导气管连接顺序从左到右J接
(2)装置②用以检验SO2的还原性,所盛试剂最好是
(3)仪器连接好后,怎样检查装置①的气密性,简述操作要点
(4)书写①装置中反应的化学方程式
分析:(1)根据实验目的及各装置特点判断导管连接顺序;
(2)装置②检验二氧化硫还原性,需要使用氧化剂;装置④用于检验二氧化硫的漂白性,可以选用品红溶液;二氧化硫、硫化氢有毒,需要进行尾气处理;
(3)根据检验装置气密性采用方法进行解答;
(4)装置①用于制取氯化氢及有多孔隔板判断反应物特点,写出反应的化学方程式;装置③用于检验二氧化硫的氧化性,使用的是硫化氢气体与二氧化硫的反应.
(2)装置②检验二氧化硫还原性,需要使用氧化剂;装置④用于检验二氧化硫的漂白性,可以选用品红溶液;二氧化硫、硫化氢有毒,需要进行尾气处理;
(3)根据检验装置气密性采用方法进行解答;
(4)装置①用于制取氯化氢及有多孔隔板判断反应物特点,写出反应的化学方程式;装置③用于检验二氧化硫的氧化性,使用的是硫化氢气体与二氧化硫的反应.
解答:.解:(1)根据题意实验目的及装置特点可知,装置②③④是检验二氧化硫性质的,其中②④是课检验二氧化硫的漂白性和还原性,③用硫化氢检验二氧化硫的氧化性,所以导管的连接顺序为:J接C、B接G、H接D、E接I、F接A,
故答案为:C;B;G;E;F;A;
(2)装置②用来检验二氧化硫的还原性,所盛试剂为溴水;装置④中盛放的试剂最好是品红,装置⑤中所盛试剂最好是氢氧化钠溶液,目的是吸收尾气,避免污染环境,
故答案为:溴水;品红溶液;烧碱溶液;吸收二氧化硫或硫化氢尾气,避免污染空气;
(3)关闭K,打款分液漏斗的活塞,向漏掉中加水,当加水一定程度后,发现漏斗中水与①中试管水面保持一定液差,且一定时间不变,则①的气密性良好,
故答案为:关闭活塞K,向长颈漏斗中加水,直到长颈漏斗中液面高度高于试管中液面高度,若过一段时间水柱不下降,就证明气密性良好,反之,气密性不好;
(4)装置①有多孔隔板,便于控制反应生成硫化氢气体开始与停止,反应物应该为难溶的硫化物,可以使用硫化钡,硫化钡和盐酸反应生成氯化钡和硫化氢气体,反应的化学方程式为:BaS+2HCl=BaCl2+H2S↑;
SO2具有氧化性,能与硫化氢反应生成单质硫沉淀,欲验证SO2的氧化性,应将SO2气体通入H2S溶液生成淡黄色的硫沉淀,反应的方程式为:SO2+2H2S=3S↓+2H2O
故答案为:BaS+2HCl=BaCl2+H2S↑;2H2S+SO2=3S↓+2H2O.
故答案为:C;B;G;E;F;A;
(2)装置②用来检验二氧化硫的还原性,所盛试剂为溴水;装置④中盛放的试剂最好是品红,装置⑤中所盛试剂最好是氢氧化钠溶液,目的是吸收尾气,避免污染环境,
故答案为:溴水;品红溶液;烧碱溶液;吸收二氧化硫或硫化氢尾气,避免污染空气;
(3)关闭K,打款分液漏斗的活塞,向漏掉中加水,当加水一定程度后,发现漏斗中水与①中试管水面保持一定液差,且一定时间不变,则①的气密性良好,
故答案为:关闭活塞K,向长颈漏斗中加水,直到长颈漏斗中液面高度高于试管中液面高度,若过一段时间水柱不下降,就证明气密性良好,反之,气密性不好;
(4)装置①有多孔隔板,便于控制反应生成硫化氢气体开始与停止,反应物应该为难溶的硫化物,可以使用硫化钡,硫化钡和盐酸反应生成氯化钡和硫化氢气体,反应的化学方程式为:BaS+2HCl=BaCl2+H2S↑;
SO2具有氧化性,能与硫化氢反应生成单质硫沉淀,欲验证SO2的氧化性,应将SO2气体通入H2S溶液生成淡黄色的硫沉淀,反应的方程式为:SO2+2H2S=3S↓+2H2O
故答案为:BaS+2HCl=BaCl2+H2S↑;2H2S+SO2=3S↓+2H2O.
点评:本题考查了探究二氧化硫性质的方法,题目难度中等,注意掌握二氧化硫的化学性质及检验方法,要求学生熟悉检验装置气密性是否良好的方法,试题能够培养学生的分析、理解能力.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目