题目内容
11.七铝十二钙(12CaO•7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废铝片制备七铝十二钙的工艺如下:
(1)煅粉主要含MgO和CaO,用适量的NH4NO3溶液浸取煅粉后,镁化合物几乎不溶,该工艺中不能用(NH4)2SO4代替NH4NO3,原因是CaSO4微溶于水,用(NH4)2SO4代替NH4NO3,会生成CaSO4沉淀引起Ca2+的损失.
(2)滤液I中的阴离子有NO3-,OH-;若滤液I中仅通入CO2会生成Ca(HCO3)2,从而导致CaCO3产率降低.
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O.
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式为2Al+6H2O$\frac{\underline{\;电解\;}}{\;}$2Al(OH)3↓+3H2↑.
(5)一种可超快充电的新型铝电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为Al-3e-+7AlCl4-=4Al2Cl7-.
分析 白云石煅烧发生反应:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,MgCO3$\frac{\underline{\;高温\;}}{\;}$MgO+CO2↑,在锻粉中加入适量的NH4NO3溶液后,镁化合物几乎不溶,由于NH4NO3溶液水解显酸性,与CaO反应生成Ca(NO3)2和NH3•H2O,故过滤后溶液中含Ca(NO3)2和NH3•H2O,将CO2和NH3通入滤液I中后发生反应:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,据此分析滤液中的阴离子;若滤液Ⅰ中仅通入CO2,会造成CO2过量,废铝片加入氢氧化钠溶液反应生成偏铝酸钠溶液,用NaOH溶液可除去废Al片表面的氧化膜,电解制备Al(OH)3时,电极分别为Al片和石墨,在碳酸钠溶液中搅拌电解,得到氢氧化铝,过滤加热灼烧得到氧化铝,碳酸钙和氧化铝共混加热1500°C得到七铝十二钙,
(1)锻粉是由白云石高温煅烧而来;CaSO4微溶于水;
(2)在锻粉中加入适量的NH4NO3溶液后,镁化合物几乎不溶,由于NH4NO3溶液水解显酸性,与CaO反应生成Ca(NO3)2和NH3•H2O,故过滤后溶液中含Ca(NO3)2和NH3•H2O,将CO2和NH3通入滤液I中后发生反应:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,据此分析滤液中的阴离子;若滤液Ⅰ中仅通入CO2,会造成CO2过量,据此分析产物;
(3)氧化铝和氢氧化钠反应生成偏铝酸钠和水;
(4)用Al片和石墨作电极来制备Al(OH)3,故Al做阳极,据此分析;
(5)放电时负极电极本身Al放电,失电子,根据AlCl4-和Al2Cl7-中铝元素和氯元素的比例来确定做AlCl4-做反应物而生成Al2Cl7-.
解答 解:(1)锻粉是由白云石高温煅烧而来,在煅烧白云石时,发生反应:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,MgCO3$\frac{\underline{\;高温\;}}{\;}$MgO+CO2↑,故所得锻粉主要含MgO和CaO;CaSO4微溶于水,如果用(NH4)2SO4代替NH4NO3,会生成CaSO4沉淀引起Ca2+的损失,
故答案为:CaO;CaSO4微溶于水,用(NH4)2SO4代替NH4NO3,会生成CaSO4沉淀引起Ca2+的损失;
(2)在锻粉中加入适量的NH4NO3溶液后,镁化合物几乎不溶,由于NH4NO3溶液水解显酸性,与CaO反应生成Ca(NO3)2和NH3•H2O,故过滤后溶液中含Ca(NO3)2和NH3•H2O,将CO2和NH3通入滤液I中后发生反应:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,故滤液中的阴离子主要为NO3-,还含有OH-;若滤液Ⅰ中仅通入CO2,会造成CO2过量,则会生成Ca(HCO3)2,从而导致CaCO3产率降低,
故答案为:NO3-,OH-;Ca(HCO3)2;
(3)氧化铝和氢氧化钠反应生成偏铝酸钠和水,离子反应为Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;
(4)用Al片和石墨作电极来制备Al(OH)3,故Al做阳极,石墨做阴极,阳极反应为:Al-3e-=Al3+①,阴极上是来自于水的H+放电:2H2O+2e-=2OH-+H2↑ ②
将①×2+②×3可得总反应:2Al+6H2O$\frac{\underline{\;电解\;}}{\;}$2Al(OH)3↓+3H2↑,
故答案为:2Al+6H2O$\frac{\underline{\;电解\;}}{\;}$2Al(OH)3↓+3H2↑;
(5)放电时负极电极本身Al放电,失电子,由于AlCl4-中氯元素的含量高于Al2Cl7-中氯元素的含量,故AlCl4-做反应物而Al2Cl7-为生成物,由于其它离子不参与电极反应,故电极反应为:Al-3e-+7AlCl4-=4Al2Cl7-,
故答案为:Al-3e-+7AlCl4-=4Al2Cl7-.
点评 本题是一道非常典型的工艺流程图题,综合性较强,综合了元素化合物、电解池和原电池的知识考查,难度较大.

 阅读快车系列答案
阅读快车系列答案| A. | 加入试剂按①SO42- ②Cl- ③OH-的正确顺序可以将混合液中Cu2+、Ba2+、Ag+逐一沉淀出来加以分离 | |
| B. | 配制480mL 1.0mol•L-1的NaOH溶液时,用托盘天平称取19.2gNaOH固体 | |
| C. | 用萃取分液的方法除去酒精中的水 | |
| D. | 用可见光束照射以区别溶液和胶体 |
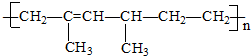
| A. | 2,4-二甲基-2-已烯 | B. | 2,4-二甲基-1,3-已二烯 | ||
| C. | 乙烯和2-甲基-1,3-戊二烯 | D. | 烯和2-甲基-1,3-丁二烯 |
| A. | Be | B. | F | C. | Br | D. | I |
| A. | 处理废水中的Cr2O72-的物质的量为nx | |
| B. | 反应中发生转移的电子数为6nxmol | |
| C. | 在FeO•FeyCrxO3中,y=3x=$\frac{3}{2}$ | |
| D. | 消耗硫酸亚铁的物质的量为n(2-x) |
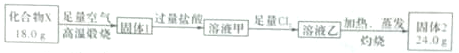
下列说法不正确的是( )
| A. | 固体2是Fe2O3 | |
| B. | 溶液甲中可能含有Fe3+ | |
| C. | X的化学式可以表示为Fe3C2 | |
| D. | X与足量的热浓硝酸反应有NO2和CO2生成 |
| A. | 酸性氧化物 | B. | 有机物 | C. | 碱性氧化物 | D. | 混合物 |
| 相关信息 | |
| A | 所处的周期数、族序数分别与其原子序数相等 |
| B | 核外有3种不同原子轨道,每个轨道容纳的电子数相等 |
| C | 基态时,2p轨道处于半充满状态 |
| D | 与C元素处于同一周期,且D的第一电离能小于C的第一电离能 |
| E | 是目前生产、生活中应用最广泛的金属 |
(1)E位于元素周期表第四 周期第Ⅷ族,其简化电子排布式为[Ar]3d64s2.
(2)D原子最外层电子排布图是

(3)A和B按照 1:1组成的相对分子质量最小的化合物甲中
①每个甲分子中含有3个σ键.
②甲气体常用作燃料电池的负极材料,写出在NaOH溶液中甲用作负极的电极反应式C2H2-10e-+14OH-=2CO32-+8H2O.
(4)A和C组成的固体化合物AC5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,写出固体化合物AC5 的电子式
 .
.(5)已知在元素周期表中存在“对角线规则”,即周期表中左上方与右下方元素它们的单质及其化合物的性质相似,如Li和Mg,试写出向BeCl2溶液中加入过量的NaOH溶液反应的化学方程式:BeCl2+4NaOH═Na2BeO2+2NaCl+2H2O.