题目内容
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是 ( )。
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | 浓硫酸有强氧化性 | 浓硫酸可用于干燥H2和CO |
| D | Fe3+有氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
D
解析

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是 ( )
| A.肯定有SO2和NO | B.肯定只有NO |
| C.可能有Cl2和O2 | D.肯定没有Cl2、NO2,可能有O2 |
实验室常用全是磨砂接口的曲颈甑制取HNO3(如图),反应的化学方程式为:NaNO3+H2SO4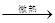 NaHSO4+HNO3↑用曲颈甑是因为HNO3
NaHSO4+HNO3↑用曲颈甑是因为HNO3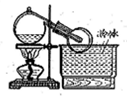
| A.会腐蚀橡胶 | B.易挥发 |
| C.易分解 | D.是强电解质 |
检验氯化氢气体中是否混有氯气,不可采用的方法是
| A.用紫色的石蕊溶液 | B.用湿润的有色布条 |
| C.将气体通入硝酸银溶液. | D.用湿润的淀粉碘化钾试纸 |
某同学用下列装置制备并检验Cl2的性质。下列说法正确的是( )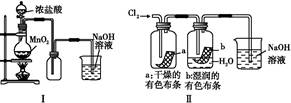
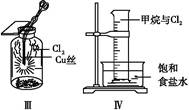
| A.Ⅰ图中:如果MnO2过量,盐酸可全部被消耗 |
| B.Ⅱ图中:湿润的有色布条褪色,证明Cl2有漂白性 |
| C.Ⅲ图中:生成棕色的固体,证明Cl2有强氧化性 |
| D.Ⅳ图中:光照后量筒中气体体积减小,说明甲烷与Cl2发生了加成反应 |
一定温度下,将Cl2缓慢通入水中。当通入的Cl2体积为V1时达到饱和,溶液中c(H+)变化如图中曲线a。已知Cl2的溶解度随温度升高而迅速降低,下列叙述中正确的是( )
| A.将饱和氯水升温,继续通入Cl2时,溶液中c(H+)变化如曲线b |
| B.在饱和氯水中通入SO2气体,溶液中c(H+)变化如曲线c |
| C.降温,继续通入Cl2时,溶液中c(H+)的变化曲线如b |
| D.在饱和氯水中加入NaOH使pH=7,所得溶液中存在c(Na+)>c(ClO-)>c(Cl-) |
通过对实验现象的观察、分析推理得出结论是化学学习的方法之一。对下列实验事实解释正确的是( )
| | 现象 | 解释 |
| A | KI淀粉溶液中通入Cl2,溶液变蓝 | Cl2能与淀粉发生显色反应 |
| B | 浓硝酸在光照条件下变黄 | 浓硝酸不稳定,生成有色产物能溶于浓硝酸 |
| C | 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后溶液的红色褪去 | BaCl2溶液具有酸性 |
| D | 向盐酸中加入浓硫酸时产生白雾 | 浓硫酸具有脱水性 |