题目内容
已知(l)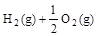 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·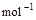
(2)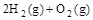 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·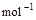
(3)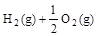 =H2O(l) △H3=c kJ·
=H2O(l) △H3=c kJ·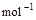
(4)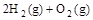 =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·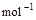
下列关系式中正确的是( )
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
C
解析试题分析:由于气态水的能量高于液态水的能量,所以等量H2在O2中完全燃烧,生成H2O(g)与生成H2O(l)放出的能量不相同,后者放出的热量多。但放热越多,△H越小,即0>b>d、0>a>c。反应放出的热量与消耗氢气的物质的量成正比,所以2a=b<0、2c=d<0,答案选C。
考点:考查反应热的有关计算和判断
点评:该题是中等难度的试题,也是高考中的常见题型、试题设计新颖,基础性强,注重答题的灵活性。有利于激发学生的学习求知欲,调动学生的学习兴趣。该题还需要明确的是在比较反应热大小时,要带着“-”和“+“进行比较。

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
已知(l)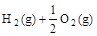 =H2O(g) ΔH1=a kJ·
=H2O(g) ΔH1=a kJ·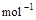
(2)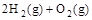 =2H2O(g) ΔH2=b kJ·
=2H2O(g) ΔH2=b kJ·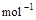
(3)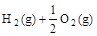 =H2O(l) ΔH3=c kJ·
=H2O(l) ΔH3=c kJ·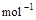
(4)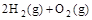 =2H2O(l) ΔH4=d kJ·
=2H2O(l) ΔH4=d kJ·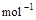
下列关系式中正确的是
| A. a<c <0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
已知
(l)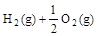 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·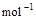
(2)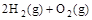 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·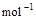
(3)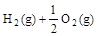 =H2O(l) △H3=c kJ·
=H2O(l) △H3=c kJ·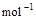
(4)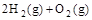 =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·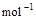
下列关系式中正确的是( )
| A.a<c <0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
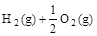 =H2O(g) ΔH1=a kJ·
=H2O(g) ΔH1=a kJ·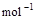
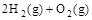 =2H2O(g) ΔH2=b kJ·
=2H2O(g) ΔH2=b kJ·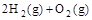 =2H2O(l) ΔH4=d kJ·
=2H2O(l) ΔH4=d kJ·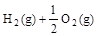 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·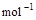
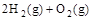 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·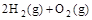 =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·