题目内容
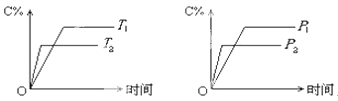
【题目】对于反应2A(g) + B(g) ![]() 2C(g)在反应过程中C的质量分WC随温度变化如图所示,试确定:
2C(g)在反应过程中C的质量分WC随温度变化如图所示,试确定:
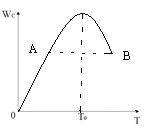
(1)T0对应的V正与V逆关系是V正___________V逆(填“>”、“<”、“=”)。
(2)A、B两点正反应速率的大小关系VA___________VB(填“>”、“<”、“=”)。
(3)温度T<T0时,Wc逐渐增大的原因是____________________;
(4)500℃条件下,该反应 K =2.33 ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正)____________v(逆)(填“>”“<”或“=”)
【答案】(1)=(2)<(3)反应还没有到达平衡,反应向正反应进行,随着温度升高,生成的C越来越多⑷>
【解析】
试题分析:(1)由图可知,温度T0前,C的质量分数增大,故未达平衡,反应向正反应进行,温度T0后,C的质量分数减小,平衡向逆反应进行,故温度T0时,反应到达平衡状态,故V正=V逆;
(2)A、B两点,各组分的浓度相同,温度越高反应速率与快,所以反应速率是VA<VB;
(3)温度T0前,反应还没有到达平衡,反应向正反应进行,随着温度升高,生成的C越来越多;
(4)测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则浓度熵Q=![]() =2<2.33,所以反应向正反应方向进行,则v(正)>v(逆)。
=2<2.33,所以反应向正反应方向进行,则v(正)>v(逆)。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目