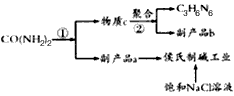
题目内容
关于氨气的实验较多,下面对这些实验的实验原理的分析中,正确的是( )
| A、氨气极易溶解于水的性质可以解释氨气的喷泉实验 | B、氨气的还原性可以解释氨气与氯化氢的反应实验 | C、铵盐的水溶性是实验室中用NH4Cl和Ca(OH)2的混合物制取氨气的原因 | D、NH3?H2O的热不稳定性可以解释实验室用加热氨水的方法制取氨气 |
分析:A、极易溶于水的气体可以做喷泉实验;
B、氨气与氯化氢的反应属于非氧化还原反应,没有元素化合价的升降;
C、用NH4Cl和Ca(OH)2的混合物制取氨气体现了铵盐可以和强碱之间反应的性质;
D、实验室用浓氨水和碱石灰混合的方法来制取氨气.
B、氨气与氯化氢的反应属于非氧化还原反应,没有元素化合价的升降;
C、用NH4Cl和Ca(OH)2的混合物制取氨气体现了铵盐可以和强碱之间反应的性质;
D、实验室用浓氨水和碱石灰混合的方法来制取氨气.
解答:解:A、氨气的喷泉实验原理:氨气极易溶于水,导致烧瓶内外气压差的出现,产生喷泉,所以该实验体现了氨气极易溶于水的性质,故A正确;
B、氨气与氯化氢的反应生成氯化铵,体现了氨气的碱性和氯化氢的酸性,该反应属于非氧化还原反应,故B错误;
C、用NH4Cl和Ca(OH)2的混合物制取氨气体现了铵盐可以和强碱之间反应的性质,不能用溶液来制取,因为氨气极易溶于水,故C错误;
D、实验室用浓氨水和碱石灰混合的方法来制取氨气,可以根据平衡NH3?H2O?NH3+H2O的移动原理来解释,故D错误.
故选A.
B、氨气与氯化氢的反应生成氯化铵,体现了氨气的碱性和氯化氢的酸性,该反应属于非氧化还原反应,故B错误;
C、用NH4Cl和Ca(OH)2的混合物制取氨气体现了铵盐可以和强碱之间反应的性质,不能用溶液来制取,因为氨气极易溶于水,故C错误;
D、实验室用浓氨水和碱石灰混合的方法来制取氨气,可以根据平衡NH3?H2O?NH3+H2O的移动原理来解释,故D错误.
故选A.
点评:氨的化学性质的灵活掌握是解答好该题的关键,注意氨气是中学阶段所学的唯一的碱性气体,这一点是考试的热点,难度不大.

练习册系列答案
相关题目