题目内容
工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g)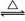 Si3N4(s)+12HCl(g) ΔH<0
Si3N4(s)+12HCl(g) ΔH<0
某温度和压强条件下,分别将0.3 mol SiCl4(g)、0.2 mol N2(g)、0.6 mol H2(g)充入2 L密闭容器内,进行上述反应,5 min达到平衡状态,所得Si3N4(s)的质量是5.60 g。
(1)H2的平均反应速率是 mol·L-1·min-1。
(2)平衡时容器内N2的浓度是 mol·L-1。
(3)SiCl4(g)的转化率是 。
(4)若按n(SiCl4)∶n(N2)∶n(H2)=3∶2∶6的投料配比,向上述容器不断扩大加料,SiCl4(g)的转化率应 (填“增大”“减小”或“不变”)。
(5)在不改变反应条件的情况下,为了提高SiCl4(g)的转化率,可通过改变投料配比的方式来实现。下列四种投料方式,其中可行的是 。
(6)达到平衡后升高温度,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
A.c(HCl)减少
B.正反应速率减慢,逆反应速率加快
C.Si3N4的物质的量减小
D.重新平衡时c(H2)/c(HCl)增大
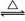 Si3N4(s)+12HCl(g) ΔH<0
Si3N4(s)+12HCl(g) ΔH<0某温度和压强条件下,分别将0.3 mol SiCl4(g)、0.2 mol N2(g)、0.6 mol H2(g)充入2 L密闭容器内,进行上述反应,5 min达到平衡状态,所得Si3N4(s)的质量是5.60 g。
(1)H2的平均反应速率是 mol·L-1·min-1。
(2)平衡时容器内N2的浓度是 mol·L-1。
(3)SiCl4(g)的转化率是 。
(4)若按n(SiCl4)∶n(N2)∶n(H2)=3∶2∶6的投料配比,向上述容器不断扩大加料,SiCl4(g)的转化率应 (填“增大”“减小”或“不变”)。
(5)在不改变反应条件的情况下,为了提高SiCl4(g)的转化率,可通过改变投料配比的方式来实现。下列四种投料方式,其中可行的是 。
| 选项 | 投料方式 |
| A | n(SiCl4)∶n(N2)∶n(H2)=1∶1∶2 |
| B | n(SiCl4)∶n(N2)∶n(H2)=" " 1∶2∶2 |
| C | n(SiCl4)∶n(N2)∶n(H2)=" " 3∶2∶2 |
| D | n(SiCl4)∶n(N2)∶n(H2)=" " 2∶1∶3 |
(6)达到平衡后升高温度,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
A.c(HCl)减少
B.正反应速率减慢,逆反应速率加快
C.Si3N4的物质的量减小
D.重新平衡时c(H2)/c(HCl)增大
(1)0.048 (2)0.06 (3)40% (4)减小 (5)A、B (6)A、C、D
依据“三部曲”计算
3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g)
Si3N4(s)+12HCl(g)
 : 0.15 0.1 0.3 0
: 0.15 0.1 0.3 0
 : 0.06 0.04 0.12 0.24
: 0.06 0.04 0.12 0.24
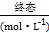 : 0.09 0.06 0.18 0.24
: 0.09 0.06 0.18 0.24
(4)相当于加压,平衡左移;(5)A、B、C、D的投料比分别为3∶3∶6、3∶6∶6、3∶2∶2、3∶1.5∶4.5,A、B、C、D分别相当于在3∶2∶6的投料配比基础上增加N2、增加N2、减少H2、减少N2和H2;(6)升高温度不论平衡向哪个方向移动,正逆反应速率均增大,B错误;升高温度,平衡左移,c(H2)增大,c(HCl)减小,A、C、D正确
3SiCl4(g)+2N2(g)+6H2(g)
 Si3N4(s)+12HCl(g)
Si3N4(s)+12HCl(g) : 0.15 0.1 0.3 0
: 0.15 0.1 0.3 0 : 0.06 0.04 0.12 0.24
: 0.06 0.04 0.12 0.24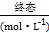 : 0.09 0.06 0.18 0.24
: 0.09 0.06 0.18 0.24(4)相当于加压,平衡左移;(5)A、B、C、D的投料比分别为3∶3∶6、3∶6∶6、3∶2∶2、3∶1.5∶4.5,A、B、C、D分别相当于在3∶2∶6的投料配比基础上增加N2、增加N2、减少H2、减少N2和H2;(6)升高温度不论平衡向哪个方向移动,正逆反应速率均增大,B错误;升高温度,平衡左移,c(H2)增大,c(HCl)减小,A、C、D正确

练习册系列答案
相关题目
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
 CH3OH(g),其他条件不变,在300 ℃和500 ℃时,甲醇物质的量n(CH3OH)反应时间t的变化曲线如图所示,下列说法正确的是( )
CH3OH(g),其他条件不变,在300 ℃和500 ℃时,甲醇物质的量n(CH3OH)反应时间t的变化曲线如图所示,下列说法正确的是( )
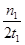 mol·L-1·min-1
mol·L-1·min-1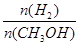 减小
减小 2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2 L的密闭容器中反应时N2的物质的量随时间的变化曲线,图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2 L的密闭容器中反应时N2的物质的量随时间的变化曲线,图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。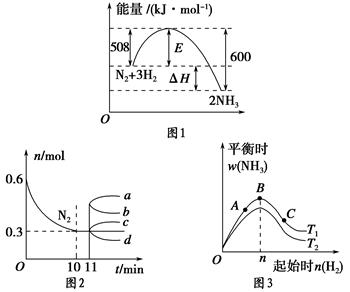

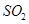 b.
b.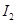 c.
c. d.HI
d.HI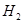 的物质的量随时间的变化如图所示。0~2min内的平均反应速率
的物质的量随时间的变化如图所示。0~2min内的平均反应速率 _________。
_________。
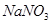 b.
b.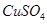 c.
c. d.
d.
 X(g)+Y(?) ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
X(g)+Y(?) ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
 cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是
cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是
 C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是