题目内容
【题目】溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.
(1)写出溴乙烷在NaOH水溶液中的反应方程式:反应类型 . 某同学取少量溴乙烷与NaOH水溶液反应后的混合溶液,向其中滴加AgNO3 溶液,加热,产生少量沉淀.该同学由此得出溴乙烷与NaOH水溶液反应,生成了溴化钠,你认为是否合理,原因: .
(2)写出溴乙烷在NaOH乙醇溶液中的反应方程式反应类型 . 反应中生成的气体可以用上图所示装置检验,现象是 , 水的作用是 . 除高锰酸钾酸性溶液外,还可以用检验生成的气体,此时还有必要将气体先通入水中吗?(填“有”或“没有”)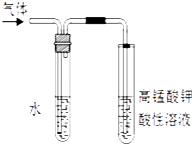
【答案】
(1)CH3CH2Br+NaOH ![]() CH3CH2OH+NaBr;取代反应;不合理,没有用硝酸中和氢氧化钠溶液
CH3CH2OH+NaBr;取代反应;不合理,没有用硝酸中和氢氧化钠溶液
(2)CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O;消去反应;溶液褪色;吸收乙醇;溴水;没有
CH2=CH2↑+NaBr+H2O;消去反应;溶液褪色;吸收乙醇;溴水;没有
【解析】解:(1)CH3CH2Br和NaOH水溶液加热时,二者发生取代反应生成乙醇和NaBr,反应方程式为CH3CH2Br+NaOH ![]() CH3CH2OH+NaBr;检验溴乙烷中含有溴元素,卤代烃水解后,加入硝酸酸化的硝酸银,硝酸酸化目的中和碱,否则生成氢氧化银沉淀, 故答案为:CH3CH2Br+NaOH
CH3CH2OH+NaBr;检验溴乙烷中含有溴元素,卤代烃水解后,加入硝酸酸化的硝酸银,硝酸酸化目的中和碱,否则生成氢氧化银沉淀, 故答案为:CH3CH2Br+NaOH ![]() CH3CH2OH+NaBr;取代反应;不合理,没有用硝酸中和氢氧化钠溶液;(2)加热条件下,溴乙烷和NaOH醇溶液发生消去反应生成乙烯,反应方程式为CH3CH2Br+NaOH
CH3CH2OH+NaBr;取代反应;不合理,没有用硝酸中和氢氧化钠溶液;(2)加热条件下,溴乙烷和NaOH醇溶液发生消去反应生成乙烯,反应方程式为CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O;
CH2=CH2↑+NaBr+H2O;
乙烯气体不溶于水,高锰酸钾能氧化乙烯,所以,它能使高锰酸钾溶液褪色,溴的四氯化碳溶液能和乙烯发生加成反应,所以,乙烯也能使溴水褪色,因装置1中用水,目的是防止乙醇和高锰酸钾反应,而溴与乙醇不反应,所以,无须用水;
故答案为:CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O,消去反应,溶液褪色,吸收乙醇,溴水,没有;
CH2=CH2↑+NaBr+H2O,消去反应,溶液褪色,吸收乙醇,溴水,没有;
(1)CH3CH2Br和NaOH水溶液加热时,二者发生取代反应生成乙醇;检验卤素原子必须中和过量的碱;(2)加热条件下,溴乙烷和NaOH醇溶液发生消去反应生成乙烯;根据乙烯的不饱和性,能被高锰酸钾溶液氧化、能和乙烯加成反应,溶液褪色,乙醇能被高锰酸钾溶液氧化,溶液褪色,乙醇不能和乙烯反应;